Lý thuyết Hóa 11 Bài 7 Kết nối tri thức, Chân trời sáng tạo, Cánh diều
Haylamdo biên soạn và sưu tầm tóm tắt Lý thuyết Hóa học 11 Bài 7 Kết nối tri thức, Chân trời sáng tạo, Cánh diều hay, ngắn gọn giúp học sinh lớp 11 nắm vững kiến thức trọng tâm, ôn tập để học tốt Hóa học 11 Bài 7.
Lý thuyết Hóa học 11 Bài 7 (sách mới cả ba sách)
Lời giải sgk Hóa học 11 Bài 7:
(Kết nối tri thức) Giải Hóa 11 Bài 7: Sulfur và sulfur dioxide
(Cánh diều) Giải Hóa 11 Bài 7: Sulfuric acid và muối sulfate
(Chân trời sáng tạo) Giải Hóa 11 Bài 7: Sulfuric acid và muối sulfate
Lưu trữ: Lý thuyết Hóa 11 Bài 7: Nitơ (sách cũ)
I. Cấu tạo phân tử
- Nhóm VA có cấu hình electron ngoài cùng là: ns2np3.
- Nên vừa thể hiện được tính oxh và tính khử.
- Cấu hình electron của N2: 1s22s22p3.
- CTCT: N ≡ N.
- CTPT: N2.
- Số oxh của N2: -3, 0, +1, +2, +3, +4, +5.
II. Tính chất vật lý
- Là chất khí không màu, không mùi, không vị, hơi nhẹ hơn không khí (d = 28/29), hóa lỏng ở -196 ºC.
- Nitơ ít tan trong nước, hoá lỏng và hoá rắn ở nhiệt độ rất thấp. Không duy trì sự cháy và sự hô hấp (không độc).
III. Tính chất hóa học
- Nitơ có các số oxi hoá: -3, 0, +1, +2, +3, +4, +5.
- N2 có số oxi hoá 0 nên vừa thể hiện tính oxi hoá và tính khử.
- Nitơ có EN N = 946 kJ/mol, ở nhiệt độ thường nitơ khá trơ về mặt hóa học nhưng ở nhiệt độ cao hoạt động hơn.
- Nitơ thể hiện tính oxi hóa và tính khử, tính oxi hóa đặc trưng hơn.
1. Tính oxi hoá: Phân tử nitơ có liên kết ba rất bền, nên nitơ khá trơ về mặt hóa học ở nhiệt độ thường.
a. Tác dụng với hidro
Ở nhiệt độ cao, áp suất cao và có xúc tác. Nitơ phản ứng với hidro tạo amoniac.
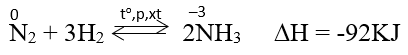
b. Tác dụng với kim loại
- Ở nhiệt độ thường nitơ chỉ tác dụng với liti tạo liti nitrua: 6Li + N2 → 2Li3N.
- Ở nhiệt độ cao, nitơ tác dụng với nhiều kim loại: 3Mg + N2 → Mg3N2 (magie nitrua).
Lưu ý: Các nitrua dễ bị thủy phân tạo NH3.
Nitơ thể hiện tính oxi hoá khi tác dụng với nguyên tố có độ âm điện nhỏ hơn.
2. Tính khử
- Ở nhiệt độ cao (3000 ºC) Nitơ phản ứng với oxi tạo nitơ monoxit.
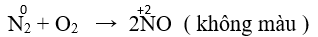
- Ở điều kiện thường, nitơ monoxit tác dụng với oxi không khí tạo nitơ đioxit màu nâu đỏ.
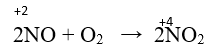
Nitơ thể hiện tính khử khi tác dụng với nguyên tố có độ âm điện lớn hơn.
- Các oxit khác của nitơ: N2O, N2O3, N2O5 không điều chế được trực tiếp từ nitơ và oxi.
Ghi nhớ: Nitơ thể hiện tính khử khi tác dụng với các nguyên tố có độ âm điện lớn hơn. Thể hiện tính oxi hóa khi tác dụng với các nguyên tố có độ âm điện lớn hơn.

IV. Trạng thái tự nhiên
Trong tự nhiên, nito tồn tại ở dạng tự do và dạng hợp chất.
- Ở dạng tự do, nito chiếm 80% thể tích không khí.
- Ở dạng hợp chất, nito có nhiều trong khoáng vật NaNO3 có tên là diêm tiêu natri.
Ngoài ra nito có trong thành phần của protein, axit ucleic, … và nhiều hợp chất hữu khác.
V. Ứng dụng và điều chế
1. Ứng dụng
- Nitơ là thành phần dinh dưỡng chính của thực vật.
- Tổng hợp amoniac để điều chế phân đạm, axit nitric …
- Được dùng làm môi trường trơ trong công nghiệp.
- Nitơ lỏng được dùng để bảo quản máu và các mẫu sinh học khác.
2. Điều chế.
a. Trong công nghiệp
Chưng cất phân đoạn không khí lỏng, thu nitơ ở -196 ºC, vận chuyển trong các bình thép, nén dưới áp suất 150 at.
b. Trong phòng thí nghiệm
Đun dung dịch bão hòa muối amoni nitrit (Hỗn hợp NaNO2 và NH4Cl):