150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải chi tiết (cơ bản) - Hoá học lớp 12
150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải chi tiết (cơ bản)
Với 150 câu trắc nghiệm Crom, Sắt, Đồng có lời giải chi tiết (cơ bản) Hoá học lớp 12 tổng hợp 150 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Crom, Sắt, Đồng từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

Câu 1. Trong các cặp kim loại sau: (1) Mg, Fe ; (2) Fe, Cu ; (3) Fe, Ag . Cặp kim loại khi tác dụng với dung dịch HNO3 có thể tạo ra dung dịch chứa tối đa 3 muối (không kể trường hợp tạo NH4NO3) là:
A. (1)
B. (1) và (2)
C. (2) và (3)
D. (1) và (2) và (3)
Lời giải:
(1) Phản ứng với HNO3 thì Mg phản ứng trước, sau đến sắt, nếu dư sắt thì 3 muối
(2) Phản ứng với HNO3 thì Fe phản ứng trước nếu Fe và Cu dư thì có thể tạo 3 muối.
(3) Không có trường hợp nào do Ag+ có tính oxi hóa mạnh hơn Fe3+... hơn nữa chỉ tạo ra Fe3+
→ Đáp án B
Câu 2. Cho phản ứng: aFe + bHNO3 → cFe(NO3)3 + dNO + eH2O
Các hệ số a, b, c, d, e là những số nguyên, đơn giản nhất. Tổng (a + b) bằng:
A. 5. B. 4.
C. 3. D. 6.
Lời giải:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
→ a + b = 5
→ Đáp án A
Câu 3. Cho bột sắt dư vào dung dịch H2SO4 loãng thu được V lít H2 (đktc) và dung dịch có chứa m1 gam muối. Mặt khác, cho bột sắt dư vào dung dịch H2SO4 đặc, nóng thu được V lít SO2 (đktc) và dd có chứa m2 gam muối. So sánh m1 và m2
A. m1 = m2
B. m1 = 0,5m2
C. m1 > m2
D. m1 < m2
Lời giải:
- Cho Fe dư + H2SO4 → m1 gam muối + V lít H2
Fe + 2H+ → Fe2+ + H2↑
nFe2+ = nH2 = V/22,4 → m1 = mFeSO4 = V/22,4 x 152 gam.
- Cho Fe + H2SO4 đặc, nóng → m2 gam muối + V lít SO2
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
nFe2(SO4)3 = 1/3 x nSO2 = 1/3 x V/22,4 mol
→ m2 = mFe2(SO4)3 = 1/3 x V/22,4 x 400 gam
→ m1 > m2
→ Đáp án C
Câu 4. Biết rằng ion Pb2+ trong dung dịch oxi hóa được Sn. Khi nhúng hai thanh kim loại Pb và Sn được nối với nhau bằng dây dẫn điện vào một dung dịch chất điện li thì
A. Cả Pb và Sn đều bị ăn mòn điện hóa.
B. Cả Pb và Sn đều không bị ăn mòn điện hóa.
C. Chỉ có Pb bị ăn mòn điện hóa.
D. Chỉ có Sn bị ăn mòn điện hóa.
Lời giải:
Sn có tính khử lớn hơn Pb nên chỉ có Sn bị ăn mòn điện hóa
→ Đáp án D
Câu 5. Hòa tan hết cùng 1 lượng Fe trong dd H2SO4 loãng(1), và H2SO4 đặc nóng (2) thì thể tích khí sinh ra trong cùng điều kiện là:
A. (1) bằng (2)
B. (1) gấp đôi (2)
C. (2) gấp rưỡi (1)
D. (2) gấp ba (1)
Lời giải:
Hòa tan hết cùng 1 lượng Fe (x mol) trong dung dịch H2SO4 loãng(1) và H2SO4 đặc, nóng (2):
Fe + H2SO4 → FeSO4 + H2↑
→ VH2 = 22,4x lít.
2Fe + 6H2SO4 đ -to→ Fe2(SO4)3 + 3SO2 + 6H2O
VSO2 = 3/2.x.22,4 = 33,6l
⇒ Thể tích khí sinh ra trong cùng điều kiện (2) gấp rưỡi (1)
→ Đáp án C
Câu 6. Để làm sạch một loại thuỷ ngân có lẫn tạp chất là Zn, Sn, Pb cần khuấy loại thuỷ ngân này trong:
A. Dung dịch Zn(NO3)2
B. Dung dịch Sn(NO3)2
C. Dung dịch Pb(NO3)2
D. Dung dịch Hg(NO3)2
Lời giải:
Để làm sạch một loại thủy ngân có lẫn tạp chất Zn, Sn, Pb cần khuấy loại thủy ngân này trong Hg(NO3)2:
Zn + Hg(NO3)2 → Zn(NO3)2 + Hg↓
Sn + Hg(NO3)2 → Sn(NO3)2 + Hg↓
Pb + Hg(NO3)2 → Pb(NO3)2 + Hg↓
→ Đáp án D
Câu 7. Cho ít bột Fe vào dung dịch AgNO3 dư. Kết thúc phản ứng được dung dịch X. Dung dịch X gồm muối :
A. Fe(NO3)2
B. Fe(NO3)2; AgNO3
C. Fe(NO3)3; AgNO3
D. Fe(NO3)2; Fe(NO3)3
Lời giải:
Cho một ít bột Fe vào AgNO3 dư:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag↓
→ Dung dịch X gồm Fe(NO3)3, AgNO3
→ Đáp án C
Câu 8. Trong các hợp chất, những nguyên tố nào dưới đây có số oxi hóa đặc trưng là +2 ?
A. Au, Ni, Zn, Pb
B. Cu, Ni, Zn, Pb
C. Ag, Sn, Ni, Au
D. Ni, Zn, K, Cr
Lời giải:
Trong các hợp chất:
- Đáp án A sai vì Au có số oxi hóa đặc trưng là +3.
- Đáp án B đúng.
- Đáp án C sai vì Ag có số oxi hóa đặc trưng là +1; Au có số oxi hóa đặc trưng là +3.
- Đáp án D sai vì K có số oxi hóa đặc trưng là +1; Cr có số oxi hóa đặc trưng là +2, +3.
→ Đáp án B
Câu 9. Cho Fe dư tác dụng với dung dịch HNO3 sau phản ứng dung dịch thu được chứa những chất tan nào ?
A. HNO3; Fe(NO3)2.
B. Fe(NO3)3.
C. Fe(NO3)2.
D. Fe(NO3)2 và Fe(NO3)3.
Lời giải:
Cho Fe dư tác dụng với dung dịch HNO3:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Fe dư + 2Fe(NO3)3 → 3Fe(NO3)2
→ Sau phản ứng thu được Fe(NO3)2
→ Đáp án C
Câu 10. Thực hiện các thí nghiệm sau (ở điều kiện thường):
(a) Cho đồng kim loại vào dung dịch sắt (III) clorua.
(b) Sục khí hiđro sunfua vào dung dịch đồng (II) sunfat.
(c) Cho dung dịch bạc nitrat vào dung dịch sắt (III) clorua.
(d) Cho bột lưu huỳnh vào thủy ngân.
Số thí nghiệm xảy ra phản ứng là
A. 2 B. 1
C. 3 D. 4
Lời giải:
(a) Cu +2FeCl3 → CuCl2 + 2FeCl2
(b) H2S + CuSO4 → CuS + H2SO4
(c) 3AgNO3 + FeCl3 → 3AgCl + Fe(NO3)3
(d) S + Pb → PbS
→ Đáp án D
Câu 11. Khi để lâu trong không khí ẩm một vật bằng sắt tây (sắt tráng thiếc) bị sây sát sâu tới lớp sắt bên trong, sẽ xảy ra quá trình:
A. Fe bị ăn mòn điện hóa
B. Sn bị ăn mòn điện hóa
C. Sn bị ăn mòn hóa học
D. Fe bị ăn mòn hóa học
Lời giải:
Do Fe có tính khử lớn hơn Sn, đủ điểu kiện để xảy ra ăn mòn điện hóa nên Fe sẽ bị ăn mòn điện hóa.
→ Đáp án A
Câu 12. Ngâm một miếng sắt kim loại vào dung dịch H2SO4 loãng. Nếu thêm vào vài giọt dung dịch CuSO4 thì sẽ có hiện tượng gì:
A. Lượng khí bay ra ít hơn
B. Lượng khí bay ra không đổi
C. Lượng khí bay ra nhiều hơn
D. Lượng khí ngừng thoát ra (do Cu bám vào miếng sắt)
Lời giải:
Khi ngâm một miếng sắt kim loại vào dung dịch H2SO4 loãng. Nếu thêm vào vài giọt dung dịch CuSO4 thì:
- Ban đầu, Fe tiếp xúc trực tiếp với ion H+ của axit, sắt bị ăn mòn hóa học theo phản ứng: Fe + 2H+ → Fe2+ + H2↑
Khi H2 sinh ra bám vào bề mặt là sắt, ngăn cản tiếp xúc giữa Fe và H+, giảm tốc độ phản ứng.
- Khi thêm vài giọt CuSO4 vào, vì tính oxi hóa Cu2+ vào, vì tính oxi hóa Cu2+ > H+, nên có phản ứng: Fe + 2Cu2+ → Fe2+ + Cu.
Cu tạo ra bám vào Fe tạo thành hai điện cực (pin điện) và Fe bị ăn mòn điện hóa, vì tính khử Fe > Cu: Cực âm (Fe): Fe → Fe2+ + 2e, Cực dương (Cu): 2H+ + 2e → H2↑
Khí thoát ra ở cực Cu, nên Fe bị ăn mòn nhanh hơn.
→ Đáp án C
Câu 13. Khi điều chế Zn từ dung dịch ZnSO4 bằng phương pháp điện phân với điện cực trơ, ở anot xảy ra quá trình
A. Khử ion kẽm
B. Khử nước
C. Oxi hóa nước
D. Oxi hóa kẽm
Lời giải:
điện phân ZnSO4
- Anot: oxi hóa nước: 2H2O → 4H+ + O2 + 4e
- Catot: khử Zn2+: Zn2+ + 2e → Zn
→ Đáp án C
Câu 14. Nhúng 1 lá sắt nhỏ vào dung dịch chứa 1 trong các chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3, H2SO4 (đặc, nóng), NH4NO3. Số trường hợp phản ứng tạo muối Fe(II) là
A. 5. B. 6.
C. 3. D. 4.
Lời giải:
Nhúng 1 lá sắt nhỏ vào dung dịch chứa 1 trong các chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3, H2SO4 (đặc, nóng), NH4NO3.
Fe + 2FeCl3 → 3FeCl2
Fe + AlCl3 → không phản ứng.
Fe + CuSO4 → FeSO4 + Cu↓
Fe + Pb(NO3)2 → Fe(NO3)2 + Pb↓
Fe + 2HCl → FeCl2 + H2
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Fe + NH4NO3 → không phản ứng.
→ Số trường hợp tạo muối Fe(II) là 4.
→ Đáp án D
Câu 15. Bạc có lẫn đồng kim loại, dùng phương pháp hoá học nào sau đây để thu được bạc tinh khiết ?
A. Ngâm hỗn hợp Ag và Cu trong dung dịch AgNO3
B. Ngâm hỗn hợp Ag và Cu trong dung dịch Cu(NO3)2
C. Ngâm hỗn hợp Ag và Cu trong dung dịch HCl
D. Ngâm hỗn hợp Ag và Cu trong dung dịch H2SO4 đặc, nóng.
Lời giải:
• Bạc có lẫn đồng kim loại, để thu được bạc tinh khiết ta ngâm hỗn hợp Ag và Cu trong dung dịch AgNO3.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
→ Đáp án đúng là đáp án A.
• Nếu ta ngâm trong HCl hoặc Cu(NO3)2 thì không có tác dụng gì.
Nếu ngâm trong H2SO4 đặc, nóng thì cả hai kim loại sẽ bị tan hết.
→ Đáp án A
Câu 16. Cấu hình electron của ion Cu2+ và Cr3+ lần lượt là
A. [Ar] 3d9 và [Ar] 3d14s2.
B. [Ar] 3d74s2 và [Ar] 3d14s2.
C. [Ar] 3d9 và [Ar] 3d3.
D. [Ar] 3d74s2 và [Ar] 3d3.
Lời giải:
- Cu có Z = 29. Cấu hình e của Cu 1s22s22p63s23p63d104s1, viết gọn là [Ar]3d104s1 → Cu2+ có cấu hình e là [Ar]3d9.
- Cr có Z = 24. Cấu hình e của Cr 1s22s22p63s23p63d54s1, viết gọn là [Ar]3d54s1 → Cr3+ có cấu hình e là [Ar]3d3.
→ Đáp án C
Câu 17. Tính chất vật lí nào dưới đây không phải là tính chất của Fe kim loại?
A. Kim loại nặng, khó nóng chảy.
B. Màu vàng nâu, cứng và giòn.
C. Dẫn điện và nhiệt tốt.
D. Có tính nhiễm từ.
Lời giải:
Sắt là kim loại f
- Có màu trắng, dẻo, dễ rèn → Đáp án B sai.
- Có khối lượng lớn 7,9g/cm3, nóng chảy ở nhiệt độ 1540oC → kim loại nặng, khó nóng chảy.
- Có tính dẫn điện, dẫn nhiệt tốt.
- Có tính nhiễm từ.
→ Đáp án B
Câu 18. Những kim loại nào sau đây có thể điều chế từ oxit kim loại bằng phương pháp nhiệt luyện nhờ chất khử CO ?
A. Fe, Al, Cu
B. Mg, Zn, Fe
C. Fe, Sn, Ni
D. Al, Cr, Zn
Lời giải:
Cơ sở của phương pháp nhiệt luyện là khử những ion kim loại trong các hợp chất ở nhiệt độ cao bằng các chất khử mạnh như: C, CO, H2 hoặc kim loại Al, kim loại kiềm, kim loại kiềm thổ.
- Phương pháp nhiệt luyện được ứng dụng rộng rãi trong công nghiệp để điều chế những kim loại có độ hoạt động trung bình như Zn, Fe, Sn, Pb,...
- Đáp án A sai vì Al không điều chế bằng phương pháp nhiệt luyện.
- Đáp án B sai vì Mg không điều chế bằng phương pháp nhiệt luyện.
- Đáp án C đúng.
- Đáp án D sai vì Al không điều chế bằng phương pháp nhiệt luyện.
→ Đáp án C
Câu 19. Sắt có Z = 26. Cấu hình electron của Fe2+ là:
A. [Ar]3d44s2
B. [Ar]3d6
C. [Ar]3d54s1
D. 1s22s22p63s23p64s23d4
Lời giải:
Cấu hình của nguyên tố sắt Z = 26: 1s22s22p63s23p63d64s2
Fe → Fe2+ + 2e
Fe2+ có cấu hình: 1s22s22p63s23p63d6 → [Ar]3d6
→ Đáp án B
Câu 20. Hiện tượng gì xảy ra khi cho từ từ dung dịch NH3 vào dung dịch CuSO4?
A. Xuất hiện kết tủa màu xanh nhạt
B. Xuất hiện kết tủa màu xanh nhạt rồi tan thành dung dịch màu xanh đậm
C. Xuất hiện dung dịch màu xanh
D. Không có hiện tượng
Lời giải:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2 (xanh nhạt) + (NH4)2SO4
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2 (dung dịch xanh đậm)
→ Đáp án B
Câu 21. Phát biểu nào sau đây là sai ?
A. Nhôm là kim loại dẫn điện tốt hơn vàng.
B. Chì (Pb) có ứng dụng để chế tạo thiết bị ngăn cản tia phóng xạ.
C. Trong y học, ZnO được dùng làm thuốc giảm đau dây thần kinh, chữa bệnh eczema, bệnh ngứa.
D. Thiếc có thể dùng để phủ lên bề mặt của sắt để chống gỉ.
Lời giải:
- Đáp án B, C, D đúng.
- Đáp án A sai vì độ dẫn điện tốt Ag > Cu > Au > Al > Fe
→ Đáp án A
Câu 22. Nhận định nào không đúng về khả năng phản ứng của sắt với nước?
A. Ở nhiệt độ cao (nhỏ hơn 570oC), sắt tác dụng với nước tạo ra Fe3O4 và H2.
B. Ở nhiệt độ lớn hơn 1000oC, sắt tác dụng với nước tạo ra Fe(OH)3.
C. Ở nhiệt độ lớn hơn 570oC, sắt tác dụng với nước tạo ra FeO và H2.
D. Ở nhiệt độ thường, sắt không tác dụng với nước.
Lời giải:
Ở nhiệt độ thường, sắt không tác dụng với nước.
Ở nhiệt độ cao, sắt khử được hơi nước:
3Fe + 4H2O -to < 570oC→ Fe3O4 + 4H2
Fe + H2O -to > 570oC→ FeO + H2
→ Ở nhiệt độ lớn hơn 1000oC, sắt tác dụng với H2O tạo ra FeO
→ Đáp án B
Câu 23. Thiếc được điều chế tốt nhất bằng
A. Phương pháp thủy luyện
B. Phương pháp nhiệt luyện
C. Phương pháp điện phân nóng chảy
D. Phương pháp điện phân dung dịch
Lời giải:
Thiếc là kim loại trung bình nên phương pháp điều chế tốt nhất là phương pháp nhiệt luyện
→ Đáp án B
Câu 24. Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư. Hiện tượng quan sát được là
A. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần.
B. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần đến không đổi. Sau đó lượng kết tủa giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm.
C. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng đến không đổi.
D. xuất hiện kết tủa màu xanh nhạt.
Lời giải:
Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Cu(OH)2↓ + 4NH3 → [Cu(NH3)4](OH)2
→ Hiện tượng quan sát được là xuất hiện ↓ màu xanh nhạt, lượng ↓ tăng dần đến không đổi. Sau đó ↓ giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm
→ Đáp án B
Câu 25. Phát biểu nào sau đây không đúng ?
A. Trong môi trường kiềm, muối Cr(III) có tính khử và bị các chất oxi hoá mạnh chuyển thành muối Cr(VI).
B. Do Pb2+/Pb đứng trước 2H+/H2 trong dãy điện hoá nên Pb dễ dàng phản ứng với dung dịch HCl loãng nguội, giải phóng khí H2.
C. CuO nung nóng khi tác dụng với NH3 hoặc CO, đều thu được Cu.
D. Ag không phản ứng với dd H2SO4 loãng nhưng phản ứng với dung dịch H2SO4 đặc nóng.
Lời giải:
B sai do PbCl2 ít an bao ngoài Pb làm cho Pb không tiếp xúc được axit dẫn đến phản dừng lại ngay
→ Đáp án B
Câu 26. Từ dung dịch FeSO4 có thể điều chế được Fe bằng phương pháp nào? (các hóa chất và phương tiện có đủ)
A. Thủy luyện
B. Nhiệt luyện
C. Điện phân
D. Cả 3 phương án trên
Lời giải:
Từ dung dịch FeSO4 có thể điều chế được Fe bằng phương pháp:
- Thủy luyện: Mg + FeSO4 → MgSO4 + Fe↓
- Nhiệt luyện: FeSO4 + 2NaOH → Fe(OH)2↓ + Na2SO4
2Fe(OH)2 + 1/2 O2 -to→ Fe2O3 + 2H2O
Fe2O3 + 3CO -to→ 2Fe + 3CO2
- Điện phân: 2FeSO4 + 2H2O -dpdd→ Fe + O2 + 2H2SO4
→ Cả 3 phương pháp đều điều chế được Fe từ FeSO4
→ Đáp án D
Câu 27. Phản ứng nào sau đây chứng tỏ hợp chất Fe(II) có tính khử?
A. Fe(OH)2 -to→ FeO + H2O
B. FeO + CO -to→ Fe + CO2
C. FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
D. 2FeCl2 + Cl2 → 2FeCl3
Lời giải:
→ Đáp án D
Câu 28. Hiện tượng xảy ra khi cho từ từ dung dịch NaOH vào dung dịch ZnSO4 đến dư ?
A. Xuất hiện kết tủa trắng, không tan trong kiềm dư.
B. Đầu tiên xuất hiện kết tủa trắng, sau đó kết tủa tan dần và dung dịch trở lại trong suốt.
C. Xuất hiện kết tủa màu xanh, sau đó kết tủa tan dần khi kiềm dư.
D. Có khí mùi xốc bay ra.
Lời giải:
Hiện tượng xảy ra khi cho từ từ dung dịch NaOH vào dung dịch ZnSO4 đến dư
2NaOH + ZnSO4 → Zn(OH)2↓ + Na2SO4
2NaOHdư + Zn(OH)2 → Na2ZnO2 + 2H2O
→ Hiện tượng: đầu tiên xuất hiện ↓ trắng, sau đó ↓ tan dần và dung dịch trở lại trong suốt.
→ Đáp án B
Câu 29. Phát biểu nào sau đây không đúng?
A. Crom (VI) oxit là oxit bazơ.
B. Ancol etylic bốc cháy khi tiếp xúc với CrO3.
C. Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+.
D. Crom (III) oxit và crom (II) hiđroxit đều là chất có tính lưỡng tính.
Lời giải:
- Crom (VI) oxit là oxit bazơ không đúng vì: CrO3 là oxit axit.
- Ancol etylic bốc cháy khi tiếp xúc với CrO3: đúng vì CrO3 có tính oxi hóa mạnh.
- Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+ đúng vì dung dịch HCl không có tính oxi hóa trong khi đó Cr có 3 số oxi hóa phổ biến +2, +3, +6.
Vậy: Crom (VI) oxit là oxit bazơ là sai.
→ Đáp án A
Câu 30. Phản ứng nào sau đây sai?
A. 2Fe + 6H2SO4 đặc, nguội → Fe2(SO4)3 + 3SO2 + 6H2O
B. Fe + H2O -t > 570oC→ FeO + H2.
C. 3Fe + 4H2O -t < 570oC→ Fe3O4 + 4H2.
D. 4Fe(OH)2 + 2H2O + O2 → 4Fe(OH)3.
Lời giải:
Fe không phản ứng với H2SO4 đặc nguội.
→ Đáp án A
Câu 31. Các đồ vật bằng bạc để trong không khí lâu ngày bị xám đen do bạc phản ứng với các chất có trong không khí là
A. O2, hơi nước.
B. CO2, hơi H2O.
C. H2S, O2.
D. H2S, CO2
Lời giải:
Bạc sẽ có màu đen khi tiếp xúc với không khí có mặt H2S
4Ag + 2H2S + O2 → 2Ag2S + 2H2O
→ Đáp án C
Câu 32. Cách đây hơn hai ngàn năm, người Trung Hoa đã biết dùng sắt để chế la bàn và đến ngày nay loại la bàn đó vẫn còn được sử dụng. Nhờ tính chất vật lí nào mà sắt có ứng dụng đó ?
A. Nhiệt độ nóng chảy cao
B. Dẫn điện, dẫn nhiệt tốt
C. Có khối lượng riêng lớn
D. Có tính nhiễm từ
Lời giải:
Kim nam châm là chất sắt có từ tính thiên nhiên lấy từ trong đá. Người ta cũng sớm biết là nếu để cho một thanh kim loại chạm vào đá nam châm thì thanh kim loại cũng có đặc tính như đá nam châm, nghĩa là có khuynh hướng chỉ về một phía tương đối cố định.
Và từ tính được truyền nhận như thế có thể bị phai dần theo thời gian. Thành ra các tàu bè dùng la bàn từ thời xa xưa vẫn phải mang theo một viên đá nam châm loại tốt, để có thể nam châm hoá hay từ hóa kim la bàn khi cần. Người ta đã biết đến sự từ hóa vào khoảng thế kỷ thứ 11.
→ Nhờ tính nhiễm từ mà sắt được dùng để chế la bàn.
→ Đáp án D
Câu 33. Cho hỗn hợp X gồm Fe2O3, ZnO và Cu tác dụng với dung dịch HCl (dư) thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng, dư) thu được kết tủa:
A. Fe(OH)2 và Cu(OH)2.
B. Fe(OH)2, Cu(OH)2 và Zn(OH)2.
C. Fe(OH)3.
D. Fe(OH)3 và Zn(OH)2.
Lời giải:
Do thu được cả kết tủa nên Cu còn dư sau phản ứng với Fe3+
Như vậy, trong dung dịch Y có FeCl2, ZnCl2 và CuCl2
Cho phản ứng với NaOH thì kết tủa thu được là Fe(OH)2 và Cu(OH)2
→ Đáp án A
Câu 34. Do Ni rất cứng nên ứng dụng quan trọng nhất của Ni là?
A. dùng trong ngành luyện kim.
B. mạ lên sắt để chống gỉ cho sắt.
C. dùng làm chất xúc tác.
D. dùng làm dao cắt kính.
Lời giải:
Phần lớn niken được dùng để chế tạo hợp kim, Ni có tác dụng làm tăng độ bền, chống ăn mòn và chịu nhiệt độ cao.
- Hợp kim Inva Ni - Fe không dãn nở theo nhiệt độ, được dùng trong kĩ thuật vô tuyến,...
- Hợp kim đồng bạch Cu - Ni có tính bền vững cao, không bị ăn mòn dù trong môi trường nước biển, dùng chế tạo chân vịt tàu biển, tuabin cho động cơ máy bay phản lực.
Một phần nhỏ niken được dùng:
- Mạ lên các kim loại khác để chống ăn mòn.
- Làm chất xúc tác (bột Ni) trong nhiều phản ứng hóa học.
- Chế tạo ắc quy Cd - Ni (có hiệu điện thế 1,4 V), ăcquy Fe – Ni.
→ Ứng dụng quan trọng nhất của Ni là dùng trong ngành luyện kim
→ Đáp án A
Câu 35. Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch axit, số cặp kim loại trong đó Fe bị phá hủy trước là:
A. 4 B. 1
C. 2 D. 3
Lời giải:
Nếu trong cặp, Fe có tính khử lớn hơn thì Fe sẽ bị phá hủy trước, đó là các cặp: Fe và Pb, Fe và Sn, Fe và Ni
→ Đáp án D
Câu 36. Phát biểu nào cho dưới đây là không đúng?
A. Fe có thể tan trong dung dịch FeCl3
B. Cu có thể tan trong dung dịch FeCl3
C. Fe không thể tan trong dung dịch CuCl2
D. Cu không thể tan trong dung dịch CuCl2
Lời giải:
Có xảy ra phản ứng: Fe + CuCl2 → FeCl2 + Cu
→ Đáp án C
Câu 37. Cho Fe vào dung dịch gồm Cu(NO3)2 và AgNO3, sau khi các phản ứng xảy ra hoàn toàn thu được dung dịch X (gồm 2 muối) và chất rắn Y (gồm 2 kim loại). Bỏ qua sự thủy phân của các muối. Hai muối trong X là:
A. Fe(NO3)2 và Fe(NO3)3
B. Cu(NO3)2 và Fe(NO3)3
C. Fe(NO3)3 và AgNO3
D. Cu(NO3)2 và Fe(NO3)2
Lời giải:
Cho Fe vào dung dịch gồm Cu(NO3)2, AgNO3 → ddX gồm 2 muối và chất rắn Y gồm 2 kim loại.
Ta có thứ tự các phản ứng trong dung dịch:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag↓
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag↓
→ Dung dịch X gồm hai kim loại gồm Ag và Cu, dung dịch gồm hai muối là Fe(NO3)2 và Cu(NO3)2
→ Đáp án D
Câu 38. Nhỏ từ từ đến dư dung dịch FeSO4 đã được axit hóa bằng H2SO4 vào dung dịch KMnO4. Hiện tượng quan sát được là
A. dung dịch màu tím hồng bị nhạt dần rồi chuyển sang màu vàng
B. dung dịch màu tím hồng bị nhạt dần đến không màu
C. dung dịch màu tím hồng bị chuyển dần sang nâu đỏ
D. màu tím bị mất ngay. Sau đó dần dần xuất hiện trở lại thành dung dịch có màu hồng
Lời giải:
10FeSO4 + 8H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 2MnSO4 + 8H2O + K2SO4.
Chú ý muối Fe2(SO4)3 và FeCl3 có màu vàng
→ Đáp án A
Câu 39. Nung FeCO3 trong không khí đến khối lượng không đổi được chất rắn X. X là:
A. FeO B. Fe2O3
C. Fe3O4 D. Fe.
Lời giải:
2FeCO3 + 1/2 O2 -to→ Fe2O3 + 2CO2
→ Đáp án B
Câu 40. Để bảo vệ vỏ tàu biển bằng thép bằng phương pháp điện hóa người ta dùng kim loại nào ?
A. Cu B. Pb
C. Zn D. Sn
Lời giải:
Để chống ăn mòn, người ta dùng một kim loại có tính khử lớn hơn Fe, thường là Zn, ghép vào vỏ tàu biển bằng thép để bảo vệ vỏ tàu, như thế Zn sẽ bị ăn mòn điện hóa trước
→ Đáp án C
Câu 41. X là một hợp chất của Zn thường được dùng trong y học, với tác dụng làm thuốc giảm đau dây thần kinh, chữa bệnh eczema, bệnh ngứa,.... Chất X là
A. Zn(NO3)2 B. ZnSO4
C. ZnO D. Zn(OH)2
Lời giải:
ZnO được dùng trong y học, với tác dụng làm thuốc đau dây thần kinh, chữa bệnh eczema, bệnh ngứa,..do ZnO có tính chất làm săn da, sát khuẩn, bảo vệ, làm dịu tổn thương da,..
→ Đáp án C
Câu 42. Thêm bột sắt (dư) vào các dung dịch riêng biệt sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3 (loãng), H2SO4 (đặc nóng). Sau khi các phản ứng xảy ra hoàn toàn, số trường hợp phản ứng tạo ra muối Fe(II) là
A. 4. B. 5.
C. 6. D. 7.
Lời giải:
Nhúng 1 lá sắt nhỏ vào dung dịch chứa 1 trong các chất sau: FeCl3, AlCl3, CuSO4, Pb(NO3)2, NaCl, HCl, HNO3, H2SO4 (đặc, nóng), NH4NO3.
• Fe + 2FeCl3 → 3FeCl2
• Fe + AlCl3 → không phản ứng.
• Fe + CuSO4 → FeSO4 + Cu↓
• Fe + Pb(NO3)2 → Fe(NO3)2 + Pb↓
• Fe + 2HCl → FeCl2 + H2
• Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Fe dư + 2Fe(NO3)3 → 3Fe(NO3)2
• 2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
Fe dư + Fe2(SO4)3 → 3FeSO4
→ Số trường hợp tạo muối Fe(II) là 6
→ Đáp án C
Câu 43. Cho các ion kim loại: Zn2+, Sn2+, Ni2+, Fe2+, Pb2+. Thứ tự tính oxi hoá giảm dần là
A. Pb2+ > Sn2+ > Fe2+ > Ni2+ > Zn2+.
B. Sn2+ > Ni2+ > Zn2+ > Pb2+ > Fe2+.
C. Zn2+ > Sn2+ > Ni2+ > Fe2+ > Pb2+.
D. Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+.
Lời giải:
Thứ tự tính khử tăng dần: Pb < Sn < Ni < Fe < Zn
Nên tính oxi giảm dần: Pb2+ > Sn2+ > Ni2+ > Fe2+ > Zn2+
→ Đáp án D
Câu 44. Cho các phát biểu sau:
(a) Các kim loại kiềm đều tan tốt trong nước.
(b) Các kim loại Mg, Fe, K và Al chỉ điều chế được bằng phương pháp điện phân nóng chảy.
(c) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(d) Khi cho Mg vào dung dịch FeCl3 dư thu được kim loại Fe.
Số phát biểu đúng là:
A. 2. B. 4.
C. 1. D. 3.
Lời giải:
(a) đúng
(b) sai do Fe không phải chỉ điều chế được bằng phương pháp điện phân nóng chảy
(c) sai do K khi cho vào dung dịch sẽ phản ứng với H2O trước nên sẽ không thể khử được Ag+
(d) sai, khi cho Mg vào Fe3+ thì sẽ phản ứng theo quy tắc alpha (tạo Fe2+), do đó, khi Fe3+ đang dư thì sẽ không tạo được Fe
Như vậy, chỉ có 1 phát biểu đúng
→ Đáp án C
Câu 45. Tôn lợp nhà thường là hợp kim nào dưới đây ?
A. Sắt tráng kẽm
B. Sắt tráng thiếc
C. Sắt tráng magie
D. Sắt tráng niken
Lời giải:
Tôn lợp nhà thường là hợp kim sắt tráng kẽm, một số mạ nhôm kẽm,..để kháng nhiệt, chống ăn mòn, mang tính thẩm mỹ
→ Đáp án A
Câu 46. Cho hỗn hợp gồm a mol FeS2 và b mol Cu2S tác dụng vừa đủ với dung dịch HNO3 thì thu được dung dịch A (chứa 2 muối sunfat) và 0,8 mol khí NO là sản phẩm khử duy nhất. Tìm a và b là
A. a = 0,06; b = 0,03.
B. a = 0,12; b = 0,06.
C. a = 0,06; b = 0,12.
D. a = 0,03; b = 0,06.
Lời giải:
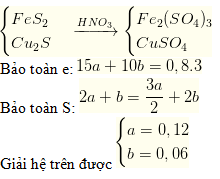
Câu 47. Các số oxi hoá có thể có của bạc trong hợp chất là
A. +1. B. +2.
C. +3. D. Cả 3 đều đúng.
Lời giải:
Trong các hợp chất, bạc có số oxi hóa phổ biến là +1, ngoài ra bạc còn có số oxi hóa là +2, +3
→ Đáp án D
Câu 48. Cho các phản ứng:
(1) Fe3O4 + H2SO4(loãng) → FeSO4 + Fe2(SO4)3 + H2O
(2) Fe + H2O → FeO + H2
(3) Fe(NO3)2 + HCl → FeCl3 + NO + H2O
(4) FeS + H2SO4(đặc nóng) → Fe2(SO4)3 + H2S + H2O
Có bao nhiêu phản ứng viết đúng ?
A. 1. B. 2.
C. 3. D. 4.
Lời giải:
(1) Đúng
(2) Đúng. Ở nhiệt độ dưới 570oC, sản phẩm Fe cộng nước là Fe3O4
(3) Sai. 9Fe(NO3)2 + 12HCl → 5Fe(NO3)3 + 4FeCl3 + 3NO + 6H2O
(4). Sai. FeS + H2SO4đn → Fe2(SO4)3 + SO2 + H2O
→ Đáp án B
Câu 49. Cho một miếng Fe vào cốc đựng H2SO4 loãng. Bọt khí H2 sẽ bay ra nhanh hơn khi thêm vào cốc trên dung dịch nào trong các dung dịch sau:
A. HgSO4 B. Na2SO4
C. Al2(SO4)3 D. MgSO4
Lời giải:
- Ban đầu, Fe tiếp xúc trực tiếp với ion H+ của axit, sắt bị ăn mòn hóa học theo phản ứng:
Fe + 2H+ → Fe2+ + H2↑
- Khi H2 sinh ra bám vào bề mặt là sắt, ngăn cản tiếp xúc giữa Fe và H+, giảm tốc độ phản ứng.
- Khi thêm vài giọt HgSO4 vào, vì tính oxi hóa Hg2+ vào, vì tính oxi hóa Hg2+ > H+, nên có phản ứng: Fe + 2Hg2+ → Fe2+ + Hg.
- Hg tạo ra bám vào Fe tạo thành hai điện cực (pin điện) và Fe bị ăn mòn điện hóa, vì tính khử Fe > Hg: Cực âm (Fe): Fe → Fe2+ + 2e, Cực dương (Hg): 2H+ + 2e → H2↑
Khí thoát ra ở cực Hg, nên Fe bị ăn mòn nhanh hơn
→ Đáp án A
Câu 50. Cho sơ đồ chuyển hóa quặng đồng thành đồng:
CuFeS2 -+O2, to→ X -+O2, to→ Y -+X, to→ Cu.
Hai chất X, Y lần lượt là:
A. Cu2O, CuO B. CuS, CuO
C. Cu2S, CuO D. Cu2S, Cu2O
Lời giải:
2CuFeS2 + 4O2 -to→ Cu2S (X) + 2FeO + 3SO2
2Cu2S + O2 → 2Cu2O (Y) + 2SO2
2Cu2O + Cu2S → 6Cu + SO2
⇒ Hai chất X, Y lần lượt là Cu2S và Cu2O.
→ Đáp án D
Câu 51. Sắt tây thường được dùng làm vỏ đồ hộp đựng thực phẩm. Hãy cho biết sắt tây là sắt được phủ bởi kim loại nào ?
A. Zn B. Sn
C. Al D. Ni
Lời giải:
Sắt tây được dùng làm vỏ đồ hộp đựng thực phẩm là sắt được tráng Sn có tác dụng chống ăn mòn, tạo vẻ đẹp và không độc hại.
→ Đáp án B
Câu 52. Hiện tượng gì xảy ra khi nhỏ một ít dung dịch KMnO4 vào dung dịch có chứa FeSO4 và H2SO4?
A. Xuất hiện màu tím hồng của dung dịch KMnO4
B. Mất màu tím hồng và xuất hiện màu vàng
C. Mất màu vàng và xuất hiện màu tím hồng
D. Cả A, B và c đều không đúng
Lời giải:
10FeSO4 + 2KMnO4 + 8H2SO4 → 5Fe2(SO4)3 + K2SO4 + MnSO4 + 8H2O
→ Đáp án B
Câu 53. Chất rắn X tác dụng với dung dịch HNO3 loãng, dư thu được dung dịch Y chỉ chứa 1 muối, axit dư và sinh ra khí NO (sản phẩm khử duy nhất). Dãy các chất nào sau đây phù hợp với X
A. Cu; CuO; Fe(OH)2.
B. CuFeS2; Fe3O4; FeO.
C. FeCO3; Fe(OH)2; Fe(OH)3.
D. Fe; Cu2O; Fe3O4.
Lời giải:
Đáp án A có CuO không tạo NO
Đáp án B có CuFeS2 chắc chắn tạo nhiều hơn 1 muối,
Đáp án C có Fe(OH)3 không tạo NO
→ Đáp án D
Câu 54. Vàng bị hoà tan trong nước cường toan tạo thành
A. AuCl và khí NO.
B. AuCl3 và khí NO2.
C. AuCl và khí NO2.
D. AuCl3 và khí NO.
Lời giải:
Au + HNO3 + 3HCl → AlCl3 + NO + 2H2O
→ Đáp án A
Câu 55. Cho các dung dịch loãng: (1) FeCl3, (2) FeCl2, (3) H2SO4, (4) HNO3, (5) hỗn hợp gồm HCl và NaNO3. Những dung dịch phản ứng được với kim loại Cu là:
A. (1), (2), (3) B. (1), (3), (5)
C. (1), (4), (5) D. (1), (3), (4)
Lời giải:
Các dung dịch phản ứng với kim loại đồng là FeCl3, HNO3, hỗn hợp gồm HCl, NaNO3. Các phản ứng:
2FeCl3 + Cu → 2FeCl2 + CuCl2
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3Cu + 2 NO3- + 8H+ → 3Cu2+ + 2NO↑ + 4H2O
→ Đáp án C
Câu 56. Kim loại nào sau đây có tác dụng hấp thụ tia gama, ngăn cản chất phóng xạ ?
A. Pt B. Pd
C. Au D. Pb
Lời giải:
Chì(Pb) có tác dụng hấp thụ tia gama nên dùng ngăn cản chất phóng xạ
→ Đáp án D
Câu 57. Nung Fe(NO3)2 trong bình kín, không có không khí, thu được sản phẩm gồm
A. FeO, NO
B. Fe2O3, NO2 và O2
C. FeO, NO2 và O2
D. FeO, NO và O2
Lời giải:
4Fe(NO3)2 → 2Fe2O3 + 4NO2 + 5O2
→ Đáp án B
Câu 58. Cho Fe dư tác dụng với dung dịch HNO3 sau phản ứng dung dịch thu được chứa những chất tan nào ?
A. HNO3; Fe(NO3)2.
B. Fe(NO3)3.
C. Fe(NO3)2.
D. Fe(NO3)2 và Fe(NO3)3.
Lời giải:
Cho Fe dư tác dụng với dung dịch HNO3:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
Fedư + 2Fe(NO3)3 → 3Fe(NO3)2
→ Sau phản ứng thu được Fe(NO3)2
→ Đáp án C
Câu 59. Cho biết số hiệu nguyên tử của Ag là 47. Cho biết vị trí của Ag trong bảng tuần hoàn:
A. Ô 47, chu kì 5, nhóm IA
B. Ô 47, chu kì 5, nhóm IB
C. Ô 47, chu kì 4, nhóm IB
D. Ô 47, chu kì 6, nhóm IIB
Lời giải:
Ag có Z = 47. Cấu hình của Ag là [Kr]4d105s1
→ Ag ở ô 47, chu kì 5, e cuối cùng điền vào phân lớp 4d nên Ag ∈ IB
→ Đáp án B
Câu 60. Cấu hình nào sau đây là cấu hình thu gọn của nguyên tử nguyên tố sắt (Z = 26) ?
A. [Ar] 3d8
B. [Ar] 3d74s1
C. [Ar] 3d64s2
D. [Ar]3d54s24p1
Lời giải:
Cấu hình của nguyên tố sắt Z = 26: 1s22s22p63s23p63d64s2 → Cấu hình thu gọn là [Ar]3d64s2
→ Đáp án C
Câu 61. Cho các chất sau (Fe, Fe2O3, Al, axit HCl, dung dịch NaOH) tác dụng với nhau từng đôi một, số phản ứng xảy ra là:
A. 3 B. 4
C. 5 D. 6
Lời giải:
1, Fe + 2HCl → FeCl2 + H2
2, Fe2O3 + 6HCl → 2FeCl3 + 3H2O
3, Al + 6HCl → 2AlCl3 + 3H2
4, Al + NaOH + H2O → NaAlO2 + 3/2 H2
5, HCl + NaOH → NaCl + H2O
→ Đáp án C
Câu 62. Hỗn hợp kim loại nào sau đây tất cả đều tham gia phản ứng trực tiếp với muối sắt (III) trong dung dịch ?
A. Na, Al, Zn
B. Fe, Mg, Cu
C. Ba, Mg, Ni
D. K, Ca, Al
Lời giải:
Nhận thấy các kim loại Na, Ba, K khi tác dụng vào các dung dịch muối sắt (III) sẽ phản ứng với nước trước tạo hidroxit, sau đó hidroxit mới phản ứng với muối sắt (III).
→ Đáp án B
Câu 63. Cho một miếng Fe vào cốc đựng H2SO4 loãng. Bọt khí H2 sẽ bay ra nhanh hơn khi thêm vào cốc trên dung dịch nào trong các dung dịch sau:
A. HgSO4 B. Na2SO4
C. Al2(SO4)3 D. MgSO4
Lời giải:
Ban đầu, Fe tiếp xúc trực tiếp với ion H+ của axit, sắt bị ăn mòn hóa học theo phản ứng:
Fe + 2H+ → Fe2+ + H2↑
Khi H2 sinh ra bám vào bề mặt là sắt, ngăn cản tiếp xúc giữa Fe và H+, giảm tốc độ phản ứng.
• Khi thêm vài giọt HgSO4 vào, vì tính oxi hóa Hg2+ vào, vì tính oxi hóa Hg2+ > H+, nên có phản ứng: Fe + Hg2+ → Fe2+ + Hg.
Hg tạo ra bám vào Fe tạo thành hai điện cực (pin điện) và Fe bị ăn mòn điện hóa, vì tính khử Fe > Hg: Cực âm (Fe): Fe → Fe2+ + 2e, Cực dương (Hg): 2H+ + 2e → H2↑
Khí thoát ra ở cực Hg, nên Fe bị ăn mòn nhanh hơn
→ Đáp án A
Câu 64. Hỗn hợp X gồm Ag, Fe, Cu. Ngâm X trong dd chỉ chứa một chất tan Y, khuấy kỹ để pư xảy ra hoàn toàn, thấy còn lại một kim loại có khối lượng không đổi so với ban đầu. Biết Y tạo kết tủa với dd BaCl2. Chất Y là
A. AgNO3. B. Fe2(SO4)3.
C. HCl. D. H2SO4.
Lời giải:
Nếu Y là AgNO3 thì thu được kim loại Ag sẽ có khối lượng lớn hơn khối lượng ban đầu
Nếu là Fe2(SO4)3 thì Fe, Cu tan, còn Ag không tan, có khối lượng không đổi
Nếu là HCl, H2SO4 thì cả Cu và Ag đều không tan nên sẽ thu được 2 kim loại
→ Đáp án B
Câu 65. Dung dịch HI có thể khử được ion nào sau đây ?
A. Fe2+ B. Fe3+
C. Cu2+ D. Al3+
Lời giải:
Ion I- có tính khử mạnh có khả năng phản ứng với Fe3+ có tính oxi hóa hình thành Fe2+
2I- + Fe3+ → Fe2+ + I2.
I- không có khả năng khử Fe2+, Cu2+, Al3+ về Fe, Cu, Al.
→ Đáp án B
Câu 66. Phát biểu nào sau đây không đúng?
A. Tính chất của sắt là tính khử.
B. Sắt tác dung với dung dịch HCl và dung dịch H2SO4 loãng cho muối sắt (II).
C. Sắt thụ động trong dung dịch HNO3 đặc nguội và H2SO4 đặc nguội.
D. Sắt tác dụng với dung dịch HNO3 loãng thu được muối và khí hiđro.
Lời giải:
Fe + 4HNO3(loãng) -to→ Fe(NO3)3 + NO + 2H2O
→ Đáp án D
Câu 67. Cho biết số hiệu nguyên tử của Zn là 30. Cho biết vị trí của Zn trong bảng tuần hoàn:
A. Ô 30, chu kì 4, nhóm IIA
B. Ô 30, chu kì 5, nhóm IIB
C. Ô 30, chu kì 4, nhóm IIB
D. Ô 30, chu kì 3 nhóm IIB
Lời giải:
Zn: [Ar] 3d104s2 ở ô 30, chu kì 4, nhóm IIB
→ Đáp án C
Câu 68. Chọn câu trả lời đúng. Trong bảng tuần hoàn các nguyên tố hoá học, vị trí của nguyên tố Fe là
A. Số thứ tự 26, chu kỳ 4, nhóm VIIB, sắt là nguyên tố kim loại nhóm B.
B. Số thứ tự 26, chu kỳ 4, nhóm VIB, sắt là nguyên tố phi kim.
C. Số thứ tự 26, chu kỳ 4, nhóm VIIIB, sắt là nguyên tố kim loại nhóm B.
D. Số thứ tự 26, chu kỳ 4, nhóm VB, sắt là kim loại nhóm B.
Lời giải:
Cấu hình của nguyên tố sắt Z = 26: 1s22s22p63s23p63d64s2 → Sắt có số thứ tự 26, chu kỳ 4.
Sắt có 8e hóa trị, e cuối cùng điền vào phần lớp d → Sắt thuộc nhóm VIIIB, là nguyên tố kim loại nhóm B
→ Đáp án C
Câu 69. Chất rắn X phản ứng với dung dịch HCl được dung dịch Y. Cho từ từ dung dịch NH3 đến dư vào dung dịch Y, ban đầu xuất hiện kết tủa xanh, sau đó kết tủa tan, thu được dung dịch màu xanh thẫm. Chất X là:
A. FeO B. Fe
C. CuO D. Cu
Lời giải:
- Rắn X phản ứng với dd HCl:
FeO + 2HCl → FeCl2 + H2O
Fe + 2HCl → FeCl2 + H2
CuO + 2HCl → CuCl2 + H2O
Cu + HCl → không xảy ra
- Dung dịch X:
FeCl2 + 2NH3 + 2H2O → Fe(OH)2 + 2NH4Cl
Fe(OH)2 + NH3 → không xảy ra
CuCl2 + 2NH3 + 2H2O → Cu(OH)2↓ + 2NH4Cl
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Dung dịch màu xanh thẫm
→ Đáp án C
Câu 70. Cho các phản ứng:
(1) Cu2O + Cu2S →
(2) Cu(NO3)2 →
(3) CuO + CO →
(4) CuO + NH3 →
Số phản ứng tạo ra kim loại Cu là:
A. 23 B. 3
C. 1 D. 4
Lời giải:
(1): 2Cu2O + Cu2S → 6Cu + SO2
(2): Cu(NO3)2 -to→ CuO + 2NO2 + 1/2 O2
(3): CuO + CO -to→ Cu + CO2
(4): 3CuO + 2NH3 -to→ 3Cu + N2 + 3H2O
→ Đáp án D
Câu 71. Muối sắt được dùng làm chất diệt sâu bọ có hại cho thực vật là
A. FeCl3 B. FeCl2
C. FeSO4 D. (NH4)SO4.Fe2(SO4)3.24H2O
Lời giải:
Muối FeSO4 được dùng làm chất diệt sâu bọ có hại cho thực vật, pha chế sơn, mực và dùng trong kĩ thuật nhuộm vải.
• Muối FeCl3 được dùng làm chất xúc tác trong một số phản ứng hữu cơ.
• Fe2(SO4) có trong phèn sắt-amoni, tức muối kép sắt(III) amoni sunfat (NH4)2SO4.Fe2(SO4)3.24H2O.
• Fe2O3 được dùng để pha chế sơn chống gỉ.
→ Đáp án C
Câu 72. Trong các phản ứng sau phản ứng nào sai:
A. Fe + 2HCldd → FeCl2 + H2
B. Fe + CuSO4dd → FeSO4 + Cu
C. Fe + Cl2 → FeCl2
D. 3Fe + 2O2 → Fe3O4
Lời giải:
Các Đáp án A, B, D đúng.
Đáp án C sai vì 2Fe + 3Cl2 → 2FeCl3
→ Đáp án C
Câu 73. Có các cặp chất sau: Cu và dung dịch FeCl3; H2S và dung dịch CuSO4; H2S và dung dịch FeCl3; dung dịch AgNO3 và dung dịch FeCl3. Số cặp chất xảy ra phản ứng ở điều kiện thường là:
A. 2 B. 3
C. 4 D. 1
Lời giải:
Các cặp chất xảy ra phản ứng
Cu + 2FeCl3 → CuCl2 + 2FeCl2
H2S + CuSO4 → CuS + H2SO4
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
3AgNO3 + FeCl3 → 3AgCl + Fe(NO3)3
→ Đáp án C
Câu 74. Trong các cặp kim loại sau, cặp kim loại nào gồm hai nguyên tố không thuộc cùng một nhóm trong bảng tuần hoàn ?
A. Ni, Zn B. Cu, Au
C. Sn, Pb D. Cu, Ag
Lời giải:
Cu và Au cùng thuộc nhóm IB
Sn và Pb cùng thuộc nhóm VIA
Cu và Ag cùng thuộc nhóm IB
Ni thuộc nhóm VIIIB, Zn thuộc nhóm IIB
→ Đáp án A
Câu 75. Phát biểu nào sau đây không đúng?
A. Trong môi trường kiềm, muối Cr(III) có tính khử và bị các chất oxi hóa mạnh chuyển thành muối Cr(VI).
B. Do Pb2+/Pb đứng trước 2H+/H2 trong dãy điện hóa nên Pb dễ dàng phản ứng với dung dịch HCl loãng nguôi, giải phóng khí H2.
C. CuO nung nóng khi tác dụng với NH3 hoặc CO, đều thu được Cu.
D. Ag không phản ứng với dung dịch H2SO4 loãng nhưng phản ứng với dung dịch H2SO4 đặc nóng.
Lời giải:
- Trong môi trường kiềm, muối Cr (III) có tính khử và bị các chất oxi hóa mạnh chuyển thành muối Cr (VI) → đáp án A đúng.
Ví dụ: 2CrCl3 + 3Cl2 + 16NaOH → 2Na2CrO4 + 12NaCl + 8H2O
- Pb2+/Pb đứng trước 2H+/H2 trong dãy điện hóa nên Pb phản ứng được vơi dung dịch HCl loãng nguội, giải phóng khí H2. Nhưng PbCl2 sinh ra ít tan bao phía ngoài Pb nên thực tế phản ứng không xảy ra. → Đáp án B sai.
- CuO nung nóng khi tác dụng với NH3 hoặc CO, đều thu được Cu → Đáp án C đúng.
3CuO + 2NH3 -to→ 3Cu + N2 + 3H2O
CuO + CO -to→ Cu + CO2
- Ag không phản ứng với dung dịch H2SO4 loãng nhưng phản ứng với dung dịch H2SO4 đặc nóng → Đáp án D đúng.
2Ag + 2H2SO4 -to→ Ag2SO4 + SO2 + 2H2O
→ Đáp án B
Câu 76. Thực hiện các phản ứng sau:
(1) Fe + dung dịch HCl
(2) Fe + Cl2
(3) dung dịch FeCl2 + Cl2
(4) Fe3O4 + dung dịch HCl
(5) Fe(NO3)2 + HCl
(6) dung dịch FeCl2 + KI
Các phản ứng có thể tạo thành FeCl3 là:
A. 1, 2, 3, 4
B. 2, 3, 4, 5
C. Chỉ 2, 3
D. Chỉ trừ 1
Lời giải:
Fe+ 2HCl → FeCl2 + H2 (1)
2Fe + 3Cl2dư → 2FeCl3 (2)
2FeCl2 + Cl2 → 2FeCl3 (3)
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O (4)
9Fe(NO3)2 + 12HCl→ 4FeCl3 + 5Fe(NO3)3 + 3NO + 6H2O (5)
FeCl2 + KI → không xảy ra phản ứng.
→ Đáp án B
Câu 77. Nhúng các thanh Fe giống nhau lần lượt vào các dung dịch: AgNO3 (1), Al(NO3)3 (2), Cu(NO3)2 (3), Fe(NO3)3 (4). Các dung dịch có thể phản ứng với Fe là
A. 1 và 3
B. 1 và 2
C. 1,3 và 4
D. 1, 2, 3 và 4
Lời giải:
Fe + 3AgNO3 (dư) → Fe(NO3)3 + 3Ag↓
Fe + Al(NO3)3 → không phản ứng.
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
→ Fe có thể phản ứng với các dung dịch (1), (3), (4)
→ Đáp án C
Câu 78. Đồng không tan được trong những dung dịch nào dưới đây?
A. dung dịch HCl có hòa tan O2
B. dung dịch FeCl3
C. dung dịch NH3 dư
D. dung dịch AgNO3
Lời giải:
∗Chú ý: Chỉ có Cu(OH)2 mới tan trong dung dịch NH3 dư do tạo phức còn Cu và CuO thì không phản ứng.
→ Đáp án C
Câu 79. Trong các kim loại sau, kim loại nào có tính dẻo cao nhất ?
A. Ag B. Al
C. Au D. Sn
Lời giải:
Tính dẻo giảm dần: Au, Ag, Al, Cu, Sn,... Người ta có thể dát được những lá vàng mỏng tới 1/20 micromet, ánh sáng có thể đi qua được.
→ Đáp án C
Câu 80. Hòa tan một oxit sắt vào dung dịch H2SO4 loãng dư được dung dịch X. Chia dung dịch X làm 2 phần bằng nhau:
- Phần 1: Cho một ít vụn Cu vào thấy tan ra và cho dung dịch có màu xanh
- Phần 2: Cho một vài giọt dung dịch KMnO4 vào thấy bị mất màu.
Oxit sắt là
A. FeO
B. Fe3O4
C. Fe2O3
D. FeO hoặc Fe2O3.
Lời giải:
Dung dịch X phản ứng được với Cu → dung dịch X chứa ion Fe3+
Dung dịch X phản ứng với KMnO4 → dung dịch X chứa ion Fe2+
Vậy oxit sắt có công thức Fe3O4.
→ Đáp án B
Câu 81. Cho phản ứng: a Fe + b HNO3 → c Fe(NO3)3 + d NO + e H2O
Các hệ số a, b, c, d, e là những số nguyên, đơn giản nhất. Tổng (a + b) bằng:
A. 5. B. 4.
C. 3. D. 6.
Lời giải:
Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O
→ a + b = 5
→ Đáp án A
Câu 82. Cho hỗn hợp có a mol Zn tác dụng với dung dịch chứa b mol Cu(NO3)2 và c mol AgNO3. Kết thúc phản ứng thu được dung dịch X và chất rắn Y. Biết a = b + 0,5c. Ta có:
A. Dung dịch X chứa 3 muối và Y chứa 2 kim loại.
B. Dung dịch X chứa 2 muối và Y chứa 2 kim loại.
C. Dung dịch X chứa 1 muối và Y có 2 kim loại.
D. Dung dịch X chứa 2 muối và Y có 1 kim loại.
Lời giải:
a = b + 0,5c ⇒ 2a = 2b + c
Như vậy, lượng Zn vừa đủ phản ứng với các chất trong dung dịch
Tóm lại, trong dung dịch X chỉ còn muối Zn(NO3)2 và trong Y có 2 kim loại là Cu và Ag
→ Đáp án C
Câu 83. Chọn câu trả lời đúng. Trong bảng tuần hoàn các nguyên tố hoá học, vị trí của nguyên tố Fe là
A. Số thứ tự 26, chu kỳ 4, nhóm VIIB, sắt là nguyên tố kim loại nhóm B.
B. Số thứ tự 26, chu kỳ 4, nhóm VIB, sắt là nguyên tố phi kim.
C. Số thứ tự 26, chu kỳ 4, nhóm VIIIB, sắt là nguyên tố kim loại nhóm B.
D. Số thứ tự 26, chu kỳ 4, nhóm VB, sắt là kim loại nhóm B
Lời giải:
Cấu hình của nguyên tố sắt Z = 26: 1s22s22p63s23p63d64s2 → Sắt có số thứ tự 26, chu kỳ 4.
Sắt có 8e hóa trị, e cuối cùng điền vào phần lớp d → Sắt thuộc nhóm VIIIB, là nguyên tố kim loại nhóm B
→ Đáp án C
Câu 84. Người Mông Cổ rất thích dùng bình làm bằng Ag để đựng sữa ngựa. Bình bằng bạc bảo quản được sữa ngựa lâu không bị hỏng là do
A. Bình làm bằng Ag bền trong không khí.
B. Ag là kim loại có tính khử rất yếu.
C. Ion Ag+ có khả năng diệt trùng, diệt khuẩn (dù có nồng độ rất nhỏ).
D. Bình làm bằng Ag, chứa các ion Ag+ có tính oxi hóa mạnh.
Lời giải:
Ion Ag+ có khả năng diệt trùng, diệt khuẩn nên thích hợp dùng làm bình đựng sữa
→ Đáp án C
Câu 85. Cho sơ đồ phản ứng sau: Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe → FeCl3
Mỗi mũi tên là một phản ứng, hãy cho biết có bao nhiêu phản ứng là phản ứng oxi hoá khử
A. 3 B. 4
C. 5 D. 6
Lời giải:
Fe -(1)→ FeCl2 -(2)→ Fe(OH)2 -(3)→ Fe(OH)3 -(4)→ Fe2O3 -(5)→ Fe -(6)→ FeCl3
Các phản ứng oxi hóa khử gồm: (1), (3), (5), (6)
→ Đáp án B
Câu 86. Hòa tan hỗn hợp gồm Fe và Cu vào dung dịch HNO3 loãng, sau phản ứng thu được chất rắn và dung dịch. Vậy trong dung dịch có các muối là:
A. Cu(NO3)2
B. Fe(NO3)2, Cu(NO3)2
C. Fe(NO3)3, Cu(NO3)2
D. Cu(NO3)2, Fe(NO3)2, HNO3
Lời giải:
Do sau phản ứng vẫn còn chất rắn nên Fe và Cu hoặc cả Fe và Cu đều còn. Khi Fe hoặc Cu còn thì Fe3+ đã chuyển hoàn toàn thành Fe2+.
→ Đáp án B
Câu 87. Nhỏ từ từ đến dư dung dịch FeSO4 đã được axit hóa bằng H2SO4 vào dung dịch KMnO4. Hiện tượng quan sát được là
A. dung dịch màu tím hồng bị nhạt dần rồi chuyển sang màu vàng
B. dung dịch màu tím hồng bị nhạt dần đến không màu
C. dung dịch màu tím hồng bị chuyển dần sang nâu đỏ
D. màu tím bị mất ngay. Sau đó dần dần xuất hiện trở lại thành dung dịch có màu hồng
Lời giải:
10FeSO4 + 8H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 2MnSO4 + 8H2O + K2SO4.
Chú ý muối Fe2(SO4)3 và FeCl3 có màu vàng
→ Đáp án A
Câu 88. Hòa tan Fe3O4 vào dung dịch HCl được dung dịch X. Chia X làm 3 phần:
- Thêm NaOH dư vào phần 1 được kết tủa Y. Lấy Y để ngoài không khí.
- Cho bột Cu vào phần 2.
- Sục Cl2 vào phần 3.
Trong các quá trình trên có số phản ứng oxi hoá - khử là
A. 2 B. 3
C. 4 D. 5
Lời giải:
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O (1)
Phần 1: FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl (2)
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl (3)
4Fe(OH)2 + O2 + 2H2O→ 4Fe(OH)3 (4)
Phần 2: 2FeCl3 + Cu → 2FeCl2 + CuCl2 (5)
Phần 3: 2FeCl2 + Cl2 → 2FeCl3 (6)
Các phản ứng oxi hóa khử là: (4), (5), (6).
→ Đáp án B
Câu 89. Phản ứng nào sau đây đã được viết không đúng?
A. 3Fe + 2O2 -to→ Fe3O4
B. 2Fe + 3Cl2 -to→ 2FeCl3
C. 2Fe + 3I2 -to→ 2FeI3
D. Fe + S -to→ FeS
Lời giải:
Nhận thấy các đáp án A, B, D đúng.
Fe khi phản ứng với I2 không tạo ra được Fe(III) mà I2 chỉ có thể oxh Fe lên Fe(II) do I2 có tính oxh nhưng không mạnh bằng các halogen khác như Cl2, Br2:
Fe + I2 -to→ FeI2
→ Đáp án C
Câu 90. Cho sơ đồ chuyển hóa quặng đồng thành đồng:
CuFeS2 -+O2, to→ X -+O2, to→ Y -+O2, to→ Ci.
Hai chất X, Y lần lượt là:
A. Cu2O, CuO B. CuS, CuO.
C. Cu2S, CuO D. Cu2S, Cu2O
Lời giải:
2CuFeS2 + 4O2 -to→ Cu2S (X) + 2FeO + 3SO2
2Cu2S + 3O2 → 2Cu2O (Y) + 2SO2
2Cu2O + Cu2S → 6Cu + SO2
⇒ Hai chất X, Y lần lượt là Cu2S và Cu2O.
→ Đáp án D
Câu 91. Sắp xếp tính khử của các kim loại theo chiều tăng dần?
A. Au, Ag, Pb, Sn, Ni, Fe, Zn
B. Au, Ag, Sn, Pb, Fe, Ni, Zn
C. Au, Ag, Sn, Pb, Ni, Fe, Zn
D. Au, Ag, Ni, Pb, Sn, Fe, Zn
Lời giải:
• Ta có dãy điện hóa
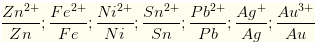
→ Tính khử của các kim loại theo chiều tăng dần là: Au < Ag < Pb < Sn < Ni < Fe < Zn.
→ Đáp án A
Câu 92. Khi điều chế FeCl2 bằng cách cho Fe tác dụng với dung dịch HCl. Để bảo quản dung dịch FeCl2 thu được không bị chuyển thành hợp chất sắt (III), người ta có thể cho thêm vào dung dịch
A. một lượng sắt dư
B. một lượng kẽm dư
C. một lượng HCl dư.
D. một lượng HNO3 dư
Lời giải:
Dung dịch FeCl2 dễ bị không khí oxi hóa thành muối Fe3+. Để bảo quản FeCl2 người ta thêm 1 lương Fe vì: Fe + 2Fe3+ → 3Fe2+
Dùng HNO3 vì HNO3 oxi hóa luôn ion Fe2+ thành Fe3+, dùng Zn sẽ tạo ra 1 lượng muối Zn2+, dùng HCl sẽ không ngăn cản quá trình tạo Fe3+.
→ Đáp án A
Câu 93. Để thu lấy Ag tinh khiết từ hỗn hợp X (gồm a mol Al2O3, b mol CuO, c mol Ag2O), người ta hòa tan X bởi dung dịch chứa (6a + 2b + 2c) mol HNO3 được dung dịch Y, sau đó thêm (giả thiết hiệu suất các phản ứng đều là 100%)
A. c mol bột Al vào Y
B. c mol bột Cu vào Y
C. 2c mol bột Al vào Y
D. 2c mol bột Cu vào Y
Lời giải:
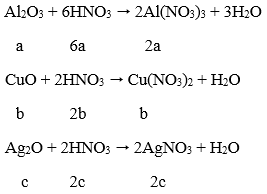
⇒ Sau phản ứng Al2O3, CuO, Ag2O và HNO3 đều hết.
Vậy dung dịch Y chứa: Al(NO3)3: 2a mol; Cu(NO3)2: b mol; AgNO3: 2c mol
Để thu được Ag từ dung dịch Y ta thêm Cu vào:
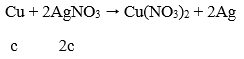
⇒ Cần c mol Cu.
→ Đáp án B
Câu 94. Cho vài giọt dung dịch H2S vào dung dịch FeCl3 hiện tượng xảy ra là
A. dung dịch xuất hiện kết tủa đen
B. có kết tủa vàng
C. kết tủa trắng hóa nâu
D. không hiện tượng gì
Lời giải:
H2S + 2FeCl3 → S↓(vàng) + 2FeCl2 + 2HCl
→ Đáp án B
Câu 95. Nhúng các thanh Fe giống nhau lần lượt vào các dung dịch: AgNO3 (1), Al(NO3)3 (2), Cu(NO3)2 (3), Fe(NO3)3 (4). Các dung dịch có thể phản ứng với Fe là
A. 1 và 3
B. 1 và 2
C. 1, 3 và 4
D. 1, 2, 3 và 4
Lời giải:
Fe + 3AgNO3 (dư) → Fe(NO3)3 + 3Ag↓
Fe + Al(NO3)3 → không phản ứng.
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu↓
Fe + 2Fe(NO3)3 → 3Fe(NO3)2
→ Fe có thể phản ứng với các dung dịch (1), (3), (4)
→ Đáp án C
Câu 96. Trong các loại quặng sắt, quặng chứa hàm lượng % Fe lớn nhất là
A. Hematit đỏ
B. Hematit nâu
C. Manhetit
D. Xiđerit
Lời giải:
Quặng hematit đỏ chứa Fe2O3 khan → %Fe = 2 x 56: 160 = 70%.
• Quặng hemantit nâu chứa Fe2O3.nH2O → %Fe < 70%.
• Quặng manhetit chứa Fe3O4 → %Fe = 3 x 56: 232 ≈ 72,41%.
• Quặng xiđerit chứa FeCO3 → %Fe = 56: 116 ≈ 48,28%
→ Quặng chứa hàm lượng sắt lớn nhất là manhetit
→ Đáp án C
Câu 97. Cho hỗn hợp Fe và Cu vào dung dịch HNO3 thấy thoát ra khí NO và NO2 thu được dung dịch X và một phần kim loại Cu không tan. Muối trong dung dịch X là
A. Fe(NO3)2, Cu(NO3)2
B. Fe(NO3)2
C. Fe(NO3)3
D. Fe(NO3)3, Cu(NO3)2
Lời giải:
Fe, Cu + HNO3 → ddX + NO, NO2 + một phần kim loại Cu không tan.
- Sau phản ứng có một phần Cu không tan → Dung dịch chỉ gồm Fe(NO3)2 và Cu(NO3)2.
Do: Cudư + 2Fe(NO3)3 → Cu(NO3)2 + 2Fe(NO3)2
→ Đáp án A
Câu 98. Nhóm nào sau đây gồm tất cả các kim loại đều khử ion Ag+ trong dung dịch AgNO3 ?
A. Zn, Fe, Ni
B. Zn, Pb, Au
C. Na, Cr, Ni
D. K, Mg, Mn
Lời giải:
• Các kim loại đều khử ion Ag+ trong dung dịch AgNO3
- Đáp án A đúng.
- Đáp án B sai vì Au không khử được Ag+.
- Đáp án C sai vì Na khi cho vào dung dịch AgNO3
2Na + 2H2O → 2NaOH + H2↑
2NaOH + 2AgNO3 → Ag2O + 2NaNO3 + H2O
- Đáp án D sai vì K khi cho vào dung dịch AgNO3
2K + 2H2O → 2KOH + H2↑
2KOH + 2AgNO3 → Ag2O + 2KNO3 + H2O
→ Đáp án A
Câu 99. Trong các phản ứng sau phản ứng nào sai:
A. Fe + 2HCldd → FeCl2 + H2
B. Fe + CuSO4dd → FeSO4 + Cu
C. Fe + Cl2 → FeCl2
D. 3Fe + 2O2 → Fe3O4
Lời giải:
Các Đáp án A, B, D đúng.
Đáp án C sai vì 2Fe + 3Cl2 → 2FeCl3
→ Đáp án C
Câu 100. Cho các phản ứng:
(1) Cu2O + Cu2S →
(2) Cu(NO3)2 →
(3) CuO + CO →
(4) CuO + NH3 →
Số phản ứng tạo ra kim loại Cu là:
A. 23 B. 3
C. 1 D. 4
Lời giải:
(1): 2Cu2O + Cu2S → 6Cu + SO2
(2): Cu(NO3)2 -to→ CuO + 2NO2 + 1/2 O2
(3): CuO + CO -to→ Cu + CO2
(4): 3CuO + 2NH3 -to→ 3Cu + N2 + 3H2O
→ Đáp án B
Câu 101. Ni tác dụng được với tất cả các chất trong dãy nào sau đây ?
A. O2, F2, Cl2, H2
B. O2, Cl2, dung dịch H2SO4 đặc nóng, dung dịch AgNO3
C. F2, Cl2, dung dịch HNO3, dung dịch Fe(NO3)2
D. S, F2, dung dịch NaCl, dung dịch Pb(NO3)2
Lời giải:
A sai, Ni không tác dụng với H2
C sai, Ni không tác dụng với Fe(NO3)2
D sai, Ni không tác dụng với NaCl
Ni tác dụng được với tất cả các chất trong B
→ Đáp án B
Câu 102. Có các hóa chất: H2O, dung dịch HCl, dung dịch NaOH, dung dịch NaCl, dung dịch KI và dung dịch K2CrO4. Crom (III) oxit tác dụng được với dung dịch nào sau đây?
A. H2O, HCl, NaOH, NaCl
B. HCl, NaOH
C. HCl, NaOH, K2CrO4
D. HCl, NaOH, KI
Lời giải:
Cr2O3 là oxit lưỡng tính nên tác dụng được với dung dịch HCl và dung dịch NaOH:
Cr2O3 + 6HCl → 2CrCl3 + 3H2O
Cr2O3 + 2NaOH + 3H2O → 2Na[Cr(OH)4]
→ Đáp án B
Câu 103. Khi vật làm bằng sắt tráng kẽm (Fe – Zn) bị ăn mòn điện hóa trong không khí ẩm, quá trình xảy ra ở điện cực âm (anot) là
A. khử Zn
B. khử H+ của môi trường
C. oxi hóa Fe
D. oxi hóa Zn
Lời giải:
Zn có tính khử mạnh hơn nên ở cực âm(anot): Zn → Zn2+ + 2e: quá trình oxi hóa Zn
→ Đáp án D
Câu 104. Khi thêm dung dịch Na2CO3 vào dung dịch FeCl3 sẽ có hiện tượng gì xảy ra ?
A. Xuất hiện kết tủa màu nâu đỏ vì xảy ra hiện tượng thủy phân
B. Dung dịchvẫn có màu nâu đỏ vì chúng không phản ứng với nhau
C. Xuất hiện kết tủa màu nâu đỏ đồng thời có hiện tượng sủi bọt khí
D. Có kết tủa nâu đỏ tạo thành sau đó lại tan do tạo khí CO2
Lời giải:
Phương trình phản ứng: 2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3↓(đỏ nâu) + 3CO2↑ + 6NaCl
→ Đáp án C
Câu 105. Một vật làm bằng hợp kim Zn-Ni đặt trong không khí ẩm. Phát biểu sai là
A. Vật bị ăn mòn điện hóa
B. Có một dòng điện từ Zn sang Ni.
C. Cực âm là Zn, xảy ra quá trình: Zn → Zn2+ + 2e
D. Zn bị ăn mòn vì Zn có tính khử mạnh hơn Ni.
Lời giải:
Khi xảy ra ăn mòn thì Zn là cực âm(anot), Ni là cực dương(catot), nên dòng điện từ Ni sang Zn
→ Đáp án B
Câu 106. Phản ứng nào sau đây sai?
A. 2Fe + 6H2SO4 đặc, nguội → Fe2(SO4)3 + 3SO2 + 6H2O
B. Fe + H2O -t > 570o→ FeO + H2.
C. 3Fe + 4H2O -t < 570o→ Fe3O4 + 4H2.
D. 4Fe(OH)2 + 2H2O + O2 → 4Fe(OH)3.
Lời giải:
Fe không phản ứng với H2SO4 đặc nguội.
→ Đáp án A
Câu 107. Tìm phát biểu đúng về Sn ?
A. Thiếc không tan trong dung dịch kiềm đặc.
B. Thiếc là kim loại có tính khử mạnh.
C. Trong tự nhiên, thiếc được bảo vệ bằng lớp màng oxit nên tương đối trơ về mặt hóa học.
D. Trong mọi hợp chất, thiếc đều có số oxi hóa +2.
Lời giải:
A Sai do Sn tan trong dung dịch kiềm đặc
B Sai, thiếc là kim loại có tính khử trung bình
C Đúng
D Sai, thiếc có số oxi hóa phổ biến là +2 và +4
→ Đáp án C
Câu 108. Thép là hợp kim của sắt chứa
A. hàm lượng cacbon lớn hơn 0,2%.
B. hàm lượng cacbon lớn hơn 2%.
C. hàm lượng cacbon nhỏ hơn 0,2%.
D. hàm lượng cacbon nhỏ hơn 2%.
Lời giải:
Thép là hợp kim của sắt và Cacbon, trong đó hàm lượng cacbon nhỏ hơn 2%
Gang là hợp kim của sắt và cacbon trong đó hàm lượng cacbon từ 2% - 5%.
→ Đáp án D
Câu 109. Hiện tượng gì xảy ra khi cho dung dịch NaOH vào ống nghiệm có chứa dung dịch FeCl2?
A. Xuất hiện màu nâu đỏ
B. Xuất hiện màu trắng xanh
C. Xuất hiện màu nâu đỏ rồi chuyển sang màu trắng xanh
D. Xuất hiện màu trắng xanh rồi chuyển sang màu nâu đỏ
Lời giải:
FeCl2 + 2NaOH → Fe(OH)2 (trắng xanh) + 2NaCl
4Fe(OH)2 + 2H2O + O2 → 4Fe(OH)3 (nâu đỏ)
→ Đáp án D
Câu 110. Cho các phát biểu sau:
(a) Các kim loại kiềm đều tan tốt trong nước.
(b) Các kim loại Mg, Fe, K và Al chỉ điều chế được bằng phương pháp điện phân nóng chảy.
(c) Các kim loại Mg, K và Fe đều khử được ion Ag+ trong dung dịch thành Ag.
(d) Khi cho Mg vào dung dịch FeCl3 dư thu được kim loại Fe.
Số phát biểu đúng là:
A. 2. B. 4.
C. 1. D. 3.
Lời giải:
(a) đúng
(b) sai do Fe không phải chỉ điều chế được bằng phương pháp điện phân nóng chảy
(c) sai do K khi cho vào dung dịch sẽ phản ứng với H2O trước nên sẽ không thể khử được Ag+
(d) sai, khi cho Mg vào Fe3+ thì sẽ phản ứng theo quy tắc alpha (tạo Fe2+), do đó, khi Fe3+ đang dư thì sẽ không tạo được Fe
Như vậy, chỉ có 1 phát biểu đúng.
→ Đáp án C
Câu 111. Cho các hoá chất:
(a) Dung dịch HNO3
(b) Dung dịch H2S có hòa tan O2
(c) O2
(d) Dung dịch FeCl3
(e) Dung dịch H2SO4 loãng
(f) Dung dịch NaCl
Kim loại Ag không tác dụng với chất nào ?
A. b, c, e
B. b, c
C. d, e, f
D. c, d, e, f
Lời giải:
Ag tác dụng được với dung dịch HNO3, H2S có hòa tan O2
Ag không tác dụng với O2, FeCl3 , H2SO4, NaCl
→ Đáp án D
Câu 112. Thí nghiệm nào sau đây có kết tủa sau phản ứng
A. Cho dung dịch NaOH đến dư vào dung dịch Cr(NO3)3.
B. Cho dung dịch HCl đến dư vào dung dịch NaAlO2 (hoặc Na[Al(OH)4])
C. Thổi CO2 đến dư vào dung dịch Ca(OH)2 .
D. Cho dung dịch NH3 đến dư vào dung dịch AlCl3.
Lời giải:
Cho dung dịch NH3 đến dư vào dung dịch AlCl3 thu được kết tủa:
3NH3 + 3H2O + AlCl3 → Al(OH)3 + 3NH4Cl
→ Đáp án D
Câu 113. Cho sơ đồ chuyển hóa giữa các hợp chất của crom:
Cr(OH)3 -+KOH→ X -+(Cl2 + KOH)→ Y -+H2SO4→ Z -+(FeSO4 + H2SO4)→ T
Các chất X, Y, Z, T theo thứ tự là:
A. KCrO2, K2CrO4, K2Cr2O7, Cr2(SO4)3.
B. K2CrO4, KCrO2, K2Cr2O7, Cr2(SO4)3.
C. KCrO2, K2Cr2O7, K2CrO4, CrSO4.
D. KCrO2, K2Cr2O7, K2CrO4, Cr2(SO4)3.
Lời giải:
Cr(OH)3 + KOH → KCrO2 (X) + 2H2O
2KCrO2 + 3Cl2 + 8KOH → 2K2CrO4 (Y) + 6KCl + 4H2O
2K2CrO4 + H2SO4 → K2Cr2O7 (Z) + K2SO4 + H2O
K2Cr2O7 (T) + 7H2SO4 + 6FeSO4 → 3Fe2(SO4)3 + Cr2(SO4)3 + 7H2O
→ Đáp án A
Câu 114. Nhận định nào không đúng về khả năng phản ứng của sắt với nước?
A. Ở nhiệt độ cao (nhỏ hơn 570oC), sắt tác dụng với nước tạo ra Fe3O4 và H2.
B. Ở nhiệt độ lớn hơn 1000oC, sắt tác dụng với nước tạo ra Fe(OH)3.
C. Ở nhiệt độ lớn hơn 570oC, sắt tác dụng với nước tạo ra FeO và H2.
D. Ở nhiệt độ thường, sắt không tác dụng với nước.
Lời giải:
Ở nhiệt độ thường, sắt không tác dụng với nước
Ở nhiệt độ cao, sắt khử được hơi nước:
Fe + H2O -t > 570oC→ FeO + H2.
3Fe + 4H2O -t > 570oC→ Fe3O4 + 4H2
→ Đáp án B
Câu 115. Tính chất vật lí nào dưới đây không phải là tính chất của Fe kim loại?
A. Kim loại nặng, khó nóng chảy.
B. Màu vàng nâu, cứng và giòn.
C. Dẫn điện và nhiệt tốt.
D. Có tính nhiễm từ.
Lời giải:
Sắt là kim loại f
- Có màu trắng, dẻo, dễ rèn → Đáp án B sai.
- Có khối lượng lớn 7,9g/cm3, nóng chảy ở nhiệt độ 1540oC → kim loại nặng, khó nóng chảy.
- Có tính dẫn điện, dẫn nhiệt tốt.
- Có tính nhiễm từ
→ Đáp án B
Câu 116. Có các nguyên liệu:
(1). Quặng sắt.
(2). Quặng Cromit.
(3). Quặng Boxit.
(4). Than cốc.
(5). Than đá.
(6). CaCO3.
(7). SiO2.
Những nguyên liệu dùng để luyện gang là:
A. (1), (3), (4), (5).
B. (1), (4), (7).
C. (1), (3), (5), (7).
D. (1), (4), (6), (7).
Lời giải:
Nguyên liệu dùng để luyện ngang là quặng sắt có chưa 30-95% oxi sắt, không chứa hoặc chứa rất ít S,P
Than cốc(không có trong tự nhiên,phải điều chế từ than mỡ) có vai trò cung cấp nhiệt khi cháy, tạo ra chất khử là CO và tạo thành gang
Chất chảy CaCO3 ở nhiệt độ cao bị phân hủy thành CaO, sao đó hóa hợp với SiO2 là chất khó nóng cháy có trong quặng sắt thành xỉ silicat dễ nóng chảy, có khối lượng riêng nhỉ nổi lên trên gang
→ Đáp án D
Câu 117. Khi thêm dung dịch Na2CO3 vào dung dịch FeCl3 sẽ có hiện tượng gì xảy ra ?
A. Xuất hiện kết tủa màu nâu đỏ vì xảy ra hiện tượng thủy phân
B. Dung dịch vẫn có màu nâu đỏ vì chúng không phản ứng với nhau
C. Xuất hiện kết tủa màu nâu đỏ đồng thời có hiện tượng sủi bọt khí
D. Có kết tủa nâu đỏ tạo thành sau đó lại tan do tạo khí CO2
Lời giải:
Phương trình phản ứng:
2FeCl3 + 3Na2CO3 + 3H2O → 2Fe(OH)3↓(đỏ nâu) + 3CO2↑ + 6NaCl
→ Đáp án C
Câu 118. Cho các chất:
(a) Dung dịch NaCN
(b) Thủy ngân
(c) Nước cường toan
(d) Dung dịch HNO3
Chất có thể hòa tan vàng là
A. b, c
B. b, c, d
C. a, b, c
D. a, b, c, d
Lời giải:
Vàng có thể tan được trong NaCN thủy ngân và nước cường toan
Au + CN- → [Au(CN)2]
Au + Hg → hỗn hống Hg-Au
Au + HNO3 + 3HCl → AuCl3 + NO + H2O
→ Đáp án C
Câu 119. Thực hiện các phản ứng sau:
(1) Fe + dung dịch HCl
(2) Fe + Cl2
(3) dung dịch FeCl2 + Cl2
(4) Fe3O4 + dung dịch HCl
(5) Fe(NO3)2 + HCl
(6) dung dịch FeCl2 + KI
Các phản ứng có thể tạo thành FeCl3 là
A. 1, 2, 3, 4
B. 2, 3, 4, 5
C. chỉ 2, 3
D. chỉ trừ 1
Lời giải:
Fe + 2HCl → FeCl2 + H2 (1)
2Fe + 3Cl2 dư → 2FeCl3 (2)
2FeCl2 + Cl2 → 2FeCl3 (3)
Fe3O4 + 8HCl → FeCl2 + 2FeCl3 + 4H2O (4)
9Fe(NO3)2 + 12HCl → 4FeCl3 + 5Fe(NO3)3 + 3NO + 6H2O (5)
FeCl2 + KI → không xảy ra phản ứng.
→ Đáp án B
Câu 120. Cho hỗn hợp Fe, cu vào dung dịch HNO3 loãng. Sau khi phản ứng xảy ra hoàn toàn thu được dung dịch chỉ chứa một chất tan và một kim loại. Chất tan đó là
Lời giải:
Fe phản ứng với HNO3 trước, sau đó Cu mới phản ứng với HNO3. Khi HNO3 hết thì Fe dư sẽ oxi hóa Fe3+ thành Fe2+. Đề cho trong dung dịch chỉ có một chất tan nên trong dung dịch phản ứng phải có Fe(NO3)2.
→ Đáp án C
Câu 121: Cho các hoá chất:
(a) Dung dịch HNO3
(b) Dung dịch H2S có hòa tan O2
(c) O2
(d) Dung dịch FeCl3
(e) Dung dịch H2SO4 loãng
(f) Dung dịch NaCl
Kim loại Ag không tác dụng với chất nào ?
A. b, c, e
B. b, c
C. d, e, f
D. c, d, e, f
Lời giải:
Ag tác dụng được với dung dịch HNO3, H2S có hòa tan O2
Ag không tác dụng với O2, FeCl3 , H2SO4, NaCl
→ Đáp án D
Câu 122. Có các cặp chất sau: Cu và dung dịch FeCl3; H2S và dung dịch CuSO4; H2S và dung dịch FeCl3; dung dịch AgNO3 và dung dịch FeCl3. Số cặp chất xảy ra phản ứng ở điều kiện thường là:
A. 2 B. 3
C. 4 D. 1
Lời giải:
Các cặp chất xảy ra phản ứng:
Cu + 2FeCl3 → CuCl2 + 2FeCl2
H2S + CuSO4 → CuS + H2SO4
H2S + 2FeCl3 → 2FeCl2 + S + 2HCl
3AgNO3 + FeCl3 → 3AgCl + Fe(NO3)3
→ Đáp án C
Câu 123. Cho Fe vào dung dịch AgNO3 dư. Sau phản ứng hoàn toàn ta thu được dung dịch X và kết tủa Y. Trong dung dịch X có chứa:
A. Fe(NO3)3, AgNO3, Fe(NO3)2.
B. Fe(NO3)3, Fe(NO3)2.
C. Fe(NO3)3, AgNO3.
D. AgNO3, Fe(NO3)2.
Lời giải:
Fe + 2AgNO3 → Fe(NO3)2 + 2Ag
Fe(NO3)2 + AgNO3 dư → Fe(NO3)3 + Ag
→ Đáp án C
Câu 124. Có các phát biểu sau:
(1) Thiếc, chì là những kim loại mà nguyên tử có 4 electron ở lớp ngoài cùng.
(2) Pb không tác dụng với dung dịch H2SO4 loãng lẫn dung dịch H2SO4 đặc nóng vì sản phẩm là PbSO4 không tan bọc ngoài kim loại, ngăn không cho phản ứng xảy ra tiếp.
(3) Sn, Pb bị hòa tan trong dung dịch kiềm, đặc nóng.
(4) Sn tác dụng với dung dịch H2SO4 loãng và dung dịch H2SO4 đặc tạo ra cùng một loại muối.
Các phát biểu đúng là:
A. 1, 2 B. 2, 3
C. 1, 3 D. 3, 4
Lời giải:
(1) đúng, thiếc: [Kr]4d105s25p2; Chì: [Kr]4f145d106s26p2; cả 2 chất thuộc nhóm IVA
(2) sai, Pb tan nhanh trong H2SO4 đặc nóng vào tạo thành muối Pb(HSO4)2
(3) đúng
(4) sai, Sn tác dụng với H2SO4 loãng được Sn(II), còn với H2SO4 đặc được Sn(IV)
→ Đáp án C
Câu 125. Cho từ từ đến dư một lượng bột sắt vào trong bình đựng một lượng nhỏ khí clo đã được đun nóng. Sau khi các phản ứng xảy ra hoàn toàn, chất rắn thu được trong bình là
A. FeCl2
B. FeCl2 và FeCl3
C. Fe và FeCl2
D. Fe và FeCl3
Lời giải:
2Fe + 3Cl2 2FeCl3
Vậy sau phản ứng chất rắn gồm Fe, FeCl3.
Chú ý phản ứng FeCl2 với Cl2 xảy ra khi FeCl2 ở trạng thái dung dịch
→ Đáp án D
Câu 126. Cho hỗn hợp X gồm Fe2O3, ZnO và Cu tác dụng với dung dịch HCl (dư) thu được dung dịch Y và phần không tan Z. Cho Y tác dụng với dung dịch NaOH (loãng, dư) thu được kết tủa
A. Fe(OH)2 và Cu(OH)2.
B. Fe(OH)2, Cu(OH)2 và Zn(OH)2.
C. Fe(OH)3.
D. Fe(OH)3 và Zn(OH)2.
Lời giải:
Do thu được cả kết tủa nên Cu còn dư sau phản ứng với Fe3+
Như vậy, trong dung dịch Y có FeCl2, ZnCl2 và CuCl2
Cho phản ứng với NaOH thì kết tủa thu được là Fe(OH)2 và Cu(OH)2
→ Đáp án A
Câu 127. Nhiệt phân hoàn toàn hỗn hợp gồm x mol AgNO3 và y mol Cu(NO3)2 được hỗn hợp khí có M = 42,5 đvC. Tỉ số x/y là:
A. 1 B. 3
C. 2 D. 4
Lời giải:
Tổng số NO2 và O2 thu được
nNO2 = x + 2y
nO2 = 0,5x + 0,5 y
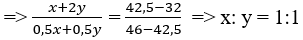
→ Đáp án A
Câu 128. Gang, thép là hợp kim của sắt. Tìm phát biểu đúng ?
A. Gang là hợp kim sắt – cacbon (5-10%).
B. Thép là hợp kim sắt – cacbon (2-5%).
C. Nguyên tắc sản xuất gang là khử sắt trong oxit bằng CO, H2 hay Al ở nhiệt độ cao.
D. Nguyên tắc sản xuất thép là oxi hóa các tạp chất trong gang (C, Si, Mn,S, P..) thành oxit, nhằm giảm hàm lượng của chúng.
Lời giải:
Gang là hợp kim sắt – cacbon (2-5%).
Thép là hợp kim sắt – cacbon (hàm lượng C < 2%)
Nguyên tắc sản xuất gang khử sắt trong oxit bằng CO ở nhiệt độ cao
→ Đáp án D
Câu 129. Để bảo quản dung dịch muối sắt (II) trong phòng thí nghiệm, người ta thường ngâm vào dung dịch đó
A. Một thanh Cu
B. Một thanh Zn
C. Một thanh Fe
D. Một thanh AI
Lời giải:
- Trong điều kiện thường Fe2+ dễ chuyển thành Fe3+
- Khi có Fe thì: Fe + 2Fe3+ → 3Fe2+
⇒ Do đó, trong dung dịch luôn có Fe2+
→ Đáp án C
Câu 130. Trong các cặp kim loại sau: (1) Mg, Fe; (2) Fe, Cu; (3) Fe, Ag . Cặp kim loại khi tác dụng với dung dịch HNO3 có thể tạo ra dung dịch chứa tối đa 3 muối (không kể trường hợp tạo NH4NO3) là:
A. (1)
B. (1) và (2)
C. (2) và (3)
D. (1) và (2) và (3)
Lời giải:
(1) Phản ứng với HNO3 thì Mg phản ứng trước, sau đến sắt, nếu dư sắt thì 3 muối
(2) Phản ứng với HNO3 thì Fe phản ứng trước nếu Fe và Cu dư thì có thể tạo 3 muối.
(3) Không có trường hợp nào do Ag+ có tính oxi hóa mạnh hơn Fe3+... hơn nữa chỉ tạo ra Fe3+
→ Đáp án B
Câu 131. Người chụp ảnh thường dùng dung dịch X để lau sạch những vết đen bám trên Ag. X là
A. Na2S2O3. B. Na2S2O7.
C. Na2CrO4. D. NaSCN.
Lời giải:
Trong nhiếp ảnh người ta dùng AgBr (không dùng AgCl kém nhạy, AgI quá nhạy với ánh sáng).
Để lau sạch những viết bám đen người ta dùng Na2S2O3 có khả năng hòa tan lớp AgBr
AgBr + 2Na2S2O3 → Na3[Ag(S2O3)2] + NaBr.
→ Đáp án A
Câu 132. Gang, thép là hợp kim của sắt. Tìm phát biểu đúng ?
A. Gang là hợp kim sắt – cacbon (5-10%).
B. Thép là hợp kim sắt – cacbon (2-5%).
C. Nguyên tắc sản xuất gang là khử sắt trong oxit bằng CO, H2 hay Al ở nhiệt độ cao.
D. Nguyên tắc sản xuất thép là oxi hóa các tạp chất trong gang (C, Si, Mn,S, P..) thành oxit, nhằm giảm hàm lượng của chúng.
Lời giải:
Gang là hợp kim sắt – cacbon (2-5%).
Thép là hợp kim sắt – cacbon (hàm lượng C < 2%)
Nguyên tắc sản xuất gang khử sắt trong oxit bằng CO ở nhiệt độ cao
→ Đáp án D
Câu 133. Nhỏ từ từ đến dư dung dịch FeSO4 đã được axit hóa bằng H2SO4 vào dung dịch KMnO4. Hiện tượng quan sát được là
A. dung dịch màu tím hồng bị nhạt dần rồi chuyển sang màu vàng
B. dung dịch màu tím hồng bị nhạt dần đến không màu
C. dung dịch màu tím hồng bị chuyển dần sang nâu đỏ
D. màu tím bị mất ngay. Sau đó dần dần xuất hiện trở lại thành dung dịch có màu hồng
Lời giải:
10FeSO4 + 8H2SO4 + 2KMnO4 → 5Fe2(SO4)3 + 2MnSO4 + 8H2O + K2SO4.
Chú ý muối Fe2(SO4)3 và FeCl3 có màu vàng
→ Đáp án A
Câu 134. Dãy gồm các chất mà khi cho từng chất tác dụng với dung dịch HI đều sinh ra sản phẩm có iot là
A. Fe2O3, Fe3O4, Fe2(SO4)3, Cl2
B. Fe(OH)3, FeO, FeCl3, Fe3O4
C. AgNO3, Na2CO3, Fe2O3, Br2
D. Fe3O4, FeO, AgNO3, FeS
Lời giải:
Ta có AgNO3 + HI → AgI↓ + HNO3 → Loại C, D
FeO + 2HI → FeI2 + H2O → Loại B
Chú ý các hợp chất Fe2O3, Fe(OH)3, Fe3O4, Fe2(SO4)3 khi tác dụng với HI sinh ra hợp chất Fe3+ có tính oxi hóa mạnh tương tác với I- trong dung dịch sinh ra I2 và Fe2+.
→ Đáp án A
Câu 135. Cho các dung dịch: Cu(NO3)2, AlCl3, AgNO3, ZnSO4, NaCl, FeCl3. Số dung dịch tạo kết tủa với dung dịch NH3 dư là:
A. 5 B. 2
C. 3 D. 4
Lời giải:
Các chất tạo kết tủa với NH3 là AlCl3 và FeCl3
→ Đáp án B
Câu 136. Phát biểu nào sau đây không đúng?
A. Crom (VI) oxit là oxit bazơ.
B. Ancol etylic bốc cháy khi tiếp xúc với CrO3.
C. Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+.
D. Crom (III) oxit và crom (II) hiđroxit đều là chất có tính lưỡng tính.
Lời giải:
- Crom (VI) oxit là oxit bazơ không đúng vì: CrO3 là oxit axit.
- Ancol etylic bốc cháy khi tiếp xúc với CrO3: đúng vì CrO3 có tính oxi hóa mạnh.
- Khi phản ứng với dung dịch HCl, kim loại Cr bị oxi hóa thành ion Cr2+ đúng vì dung dịch HCl không có tính oxi hóa trong khi đó Cr có 3 số oxi hóa phổ biến +2, +3, +6.
Vậy: Crom (VI) oxit là oxit bazơ là sai.
→ Đáp án A
Câu 137. Cho các dung dịch loãng: (1) FeCl3, (2) FeCl2, (3) H2SO4, (4) HNO3, (5) hỗn hợp gồm HCl và NaNO3. Những dung dịch phản ứng được với kim loại Cu là:
A. (1), (2), (3) B. (1), (3), (5)
C. (1), (4), (5) D. (1), (3), (4)
Lời giải:
Các dung dịch phản ứng với kim loại đồng là FeCl3, HNO3, hỗn hợp gồm HCl, NaNO3. Các phản ứng:
2FeCl3 + Cu → 2FeCl2 + CuCl2
3Cu + 8HNO3 → 3Cu(NO3)2 + 2NO + 4H2O
3Cu + 2 NO3- + 8H+ → 3Cu2+ + 2NO↑ + 4H2O
→ Đáp án C
Câu 138. Cho các phát biểu về đồng, bạc, vàng như sau:
(1) Tính khử yếu dần theo thứ tự: Cu > Ag > Au
(2) Cả 3 kim loại đều tan trong dung dịch HNO3
(3) Cả 3 kim loại đều có thể tồn tại trong tự nhiên dưới dạng đơn chất
(4) Dung dịch HNO3 chỉ hòa tan được Cu, Ag; còn không hòa tan được Au.
(5) Chỉ có Cu mới hòa tan trong dung dịch HCl, còn Ag, Au không hòa tan trong dung dịch HCl.
Số phát biểu đúng là:
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
• Tính khử yếu dần theo thứ tự: Cu > Ag > Au.
- Dung dịch HNO3 chỉ hòa tan được Cu, Ag; còn Au chỉ hòa tan trong nước cường toan ( hỗn hợp 1 thể tích HNO3 và 3 thể tích HCl đặc).
- Cả ba kim loại Cu, Ag, Au đứng sau H nên đều không hòa tan trong HCl.
- Cả ba kim loại đều có thể tồn tại trong tự nhiên dưới dạng đơn chất.
→ Có 3 phát biểu đúng là (1), (3), (4)
→ Đáp án B
Câu 139. Dãy gồm các chất mà khi cho từng chất tác dụng với dung dịch HI đều sinh ra sản phẩm có iot là
A. Fe2O3, Fe3O4, Fe2(SO4)3, Cl2
B. Fe(OH)3, FeO, FeCl3, Fe3O4
C. AgNO3, Na2.CO3, Fe2O3, Br2
D. Fe3O4, FeO, AgNO3, FeS
Lời giải:
Ta có AgNO3 + HI → AgI↓ + HNO3 → Loại C, D
FeO + 2HI → FeI2 + H2O → Loại B
Chú ý các hợp chất Fe2O3, Fe(OH)3, Fe3O4, Fe2(SO4)3 khi tác dụng với HI sinh ra hợp chất Fe3+ có tính oxi hóa mạnh tương tác với I- trong dung dịch sinh ra I2 và Fe2+.
→ Đáp án A
Câu 140. Cho vài giọt dung dịch H2S vào dung dịch FeCl3 hiện tượng xảy ra là
A. dung dịch xuất hiện kết tủa đen
B. có kết tủa vàng
C. kết tủa trắng hóa nâu
D. không hiện tượng gì
Lời giải:
H2S + 2FeCl3 → S↓(vàng) + 2FeCl2 + 2HCl
→ Đáp án B
Câu 141. Vàng bị hoà tan trong nước cường toan tạo thành
A. AuCl và khí NO.
B. AuCl3 và khí NO2.
C. AuCl và khí NO2.
D. AuCl3 và khí NO.
Lời giải:
Au + HNO3 + 3HCl → AuCl3 + NO + 2H2O
→ Đáp án A
Câu 142. Ni tác dụng được với tất cả các chất trong dãy nào sau đây ?
A. O2, F2, Cl2, H2
B. O2, Cl2, dung dịch H2SO4 đặc nóng, dung dịch AgNO3
C. F2, Cl2, dung dịch HNO3, dung dịch Fe(NO3)2
D. S, F2, dung dịch NaCl, dung dịch Pb(NO3)2
Lời giải:
A sai, Ni không tác dụng với H2
C sai, Ni không tác dụng với Fe(NO3)2
D sai, Ni không tác dụng với NaCl
Ni tác dụng được với tất cả các chất trong B
→ Đáp án B
Câu 143. Có các phát biểu về kẽm sau:
(a) Zn có thể tác dụng với các dung dịch HCl, HNO3 đặc nguội, NaOH;
(b) những đồ vật bằng Zn không bị han rỉ, không bị oxi hóa trong không khí và trong nước;
(c) có thể dùng Zn để đẩy Au ra khỏi phức xianua [Au(CN)2]- (phương pháp khai thác vàng);
(d) Zn không thể đẩy được Cu ra khỏi dung dịch CuSO4
(e) không tồn tại hợp chất ZnCO3
Số phát biểu đúng là
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
Có các phát biểu về kẽm:
- Zn có thể tác dụng với các dung dịch HCl, HNO3 đặc, nguội, NaOH.
- Zn không bị han rỉ, không bị oxi hóa trong không khí và trong nước vì trên bề mặt kẽm có màng oxit hoặc cacbonat bazơ bảo vệ.
- Zn có thể đẩy Au ra khỏi phức xianua [Au(CN)2]- (phương pháp khai thác vàng).
- Zn có thể đẩy được Cu ra khỏi dung dịch CuSO4.
- ZnCO3 tồn tại ở dạng rắn, không tồn tại ở dạng dung dịch.
→ Có 3 phát biểu đúng là (a), (b), (c)
→ Đáp án B
Câu 144. Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư. Hiện tượng quan sát được là
A. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần.
B. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng dần đến không đổi. Sau đó lượng kết tủa giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm.
C. xuất hiện kết tủa màu xanh nhạt, lượng kết tủa tăng đến không đổi.
D. xuất hiện kết tủa màu xanh nhạt.
Lời giải:
Nhỏ từ từ dung dịch NH3 vào dung dịch CuSO4 cho tới dư:
CuSO4 + 2NH3 + 2H2O → Cu(OH)2↓ + (NH4)2SO4
Cu(OH)2↓ + 4NH3 → [Cu(NH3)4](OH)2
→ Hiện tượng quan sát được là xuất hiện ↓ màu xanh nhạt, lượng ↓ tăng dần đến không đổi. Sau đó ↓ giảm dần cho tới khi tan hết thành dung dịch màu xanh đậm
→ Đáp án B
Câu 145. Cho thanh Zn tác dụng với dung dịch CuSO4, nhận định đúng là:
A. Zn bị khử còn Cu2+ bị oxi hóa
B. Zn bị oxi hóa còn Cu2+ bị khử
C. Zn và Cu đều bị oxi hóa
D. Zn và Cu đều bị khử
Lời giải:
Phương trình phản ứng: Zn + CuSO4 → ZnSO4 + Cu↓ (đỏ)
Cu sinh ra bám vào lá Zn, đồng thời lượng Cu2+ trong dung dịch giảm đi nên màu xanh giảm dần.
→ Đáp án B
Câu 146. Cho bột sắt dư vào dung dịch H2SO4 loãng thu được V lít H2 (đktc) và dung dịch có chứa m1 gam muối. Mặt khác, cho bột sắt dư vào dung dịch H2SO4 đặc, nóng thu được V lít SO2 (đktc) và dd có chứa m2 gam muối. So sánh m1 và m2.
A. m1 = m2
B. m1 = 0,5m2
C. m1 > m2
D. m1 < m2
Lời giải:
Cho Fe dư + H2SO4 → m1 gam muối + V lít H2
Fe + 2H+ → Fe2+ + H2↑
nFe2+ = nH2 = V/22,4 → m1 = mFeSO4 = V/22,4 x 152 gam.
Cho Fe + H2SO4 đặc, nóng → m2 gam muối + V lít SO2
2Fe + 6H2SO4 → Fe2(SO4)3 + 3SO2↑ + 6H2O
nFe2(SO4)3 = 1/3 x nSO2 = 1/3 x V/22,4 mol
→ m2 = mFe2(SO4)3 = 1/3 x V/22,4 x 400 gam
→ m1 > m2
→ Đáp án C
Câu 147. Cho vào ống nghiệm một ít tinh thể K2Cr2O7, sau đó cho nước vào và khuấy đều để K2Cr2O7 tan hết, thu được dung dịch X. Thêm vài giọt dung dịch KOH vào dung dịch X, thu được dung dịch Y. Màu của dung dịch X và Y lần lượt là:
A. Màu vàng và màu da cam
B. Màu nâu đỏ và màu vàng
C. Màu da cam và màu vàng
D. Màu vàng và màu nâu đỏ
Lời giải:
Trong dung dịch K2Cr2O7 (màu da cam) có cân bằng:
Cr2O72-(da cam) + H2O ⇆ 2Cr2O42-(vàng) + 2H+
Khi thêm dung dịch KOH vào, OH- trung hòa H+ làm cân bằng chuyển dịch sang phải tạo ra CrO42- có màu vàng
→ Đáp án C
Câu 148. Cho các chất sau: Cu(OH)2, AgCl, Ni, Zn(OH)2, Pb, Sn. Số chất tan trong dung dịch NH3 là:
A. 2. B. 3.
C. 4. D. 5.
Lời giải:
Cu(OH)2↓ + 4NH3 → [Cu(NH3)4](OH)2
AgCl↓ + 2NH3 → [Ag(NH3)2]Cl
Ni + NH3 → không phản ứng.
Zn(OH)2↓ + 4NH3 → [Zn(NH3)4](OH)2
Pb + NH3 → không phản ứng.
Sn + NH3 → không phản ứng.
→ Có 3 chất tan trong dung dịch NH3
→ Đáp án B
Câu 149. Để oxi hóa hoàn toàn 0,01 mol CrCl3 thành K2CrO4 bằng Cl2 khi có mặt KOH, lượng tối thiểu Cl2 và KOH tương ứng là:
A. 0,015 mol và 0,04 mol
B. 0,015 mol và 0,08 mol
C. 0,03 mol và 0,08 mol
D. 0,03 mol và 0,04 mol
Lời giải:
2CrCl3 (0,01) + 3Cl2 (0,015) + 16KOH (0,08) → 2K2CrO4 + 12KCl + 8H2O
→ Đáp án B
Câu 150. Những bức tranh cổ (vẽ bằng bột chì, thành phần chính là muối bazơ 2PbCO3.Pb(OH)2) thường có màu đen. Hãy cho biết có thể dùng chất nào dưới đây để phục hồi bức tranh cổ này ?
A. H2O2 B. HNO3
C. H2SO4 D. AgNO3
Lời giải:
- Những bức tranh cổ vẽ bằng bột chì (thành phần chính là muối bazơ 2PbCO3.Pb(OH)2). Khi để lâu bột chì tác dụng với H2S trong không khí tạo PbS màu đen.
2PbCO3.Pb(OH)2 + 3H2S → 3PbS + 2CO2 + 4H2O
- Có thể dùng H2O2 để phục hồi bức tranh này, vì PbS màu đen biến thành PbSO4 thành màu trắng theo phản ứng:
PbS + 4H2O2 → PbSO4 + 4H2O2.
→ Đáp án A

