80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (cơ bản) - Hoá học lớp 12
80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (cơ bản)
Với 80 câu trắc nghiệm Đại cương về kim loại có lời giải chi tiết (cơ bản) Hoá học lớp 12 tổng hợp 80 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập kim loại từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

Câu 1: Công thức chung của oxit kim loại thuộc nhóm IIA là
A. R2O3. B. RO2.
C. R2O. D. RO.
Lời giải:
Kim loại nhóm IIA có hóa trị II → Công thức chung của oxit kim loại thuộc nhóm IIA là RO.
→ Đáp án D
Câu 2: Nguyên tử Fe có cấu hình e là
A. [Ar]3d64s2. B. [Ar]4s13d7.
C. [Ar]3d74s1. D. [Ar]4s23d6.
Lời giải:
Nguyên tử Fe có Z = 26 → Cấu hình e của Fe là 1s22s22p63s23p63d64s2 hay [Ar]3d64s2.
→ Đáp án A
Câu 3: Cấu hình e của Cr là
A. [Ar]3d44s2. B. [Ar]4s23d4.
C. [Ar]3d54s1. D. [Ar]4s13d5.
Lời giải:
Nguyên tử Cr có Z = 24 (Có cấu hình bán bão hòa) → Cấu hình e của Cr là 1s22s22p63s23p63d54s1 hay [Ar]3d54s1.
→ Đáp án C
Câu 4: Kim loại Ni phản ứng được với tất cả các muối trong dung dịch ở dãy nào sau đây ?
A. NaCl, AlCl3, ZnCl2
B. MgSO4, CuSO4, AgNO3
C. Pb(NO3)2, AgNO3, NaCl
D. AgNO3, CuSO4, Pb(NO3)2
Lời giải:
Kim loại hoạt động có thể khử được ion kim loại kém hoạt động hơn trong dung dịch muối thành kim loại tự do.
Ni đứng trước Ag, Cu, Pb trong dãy điện hóa → Ni có thể khử được các ion kim loại trên.
Ni + 2AgNO3 → Ni(NO3)2 + 2Ag
Ni + CuSO4 → NiSO4 + Cu
Ni + Pb(NO3)2 → Ni(NO3)2 + Pb.
→ Đáp án D
Câu 5: Cho ba kim loại là Al, Fe, Cu và bốn dung dịch muối riêng biệt là ZnSO4, AgNO3, CuCl2, MgSO4. Kim loại nào tác dụng được với cả bốn dung dịch muối đã cho ?
A. Al. B. Fe.
C. Cu. D. Không kim loại nào.
Lời giải:
Không kim loại nào vì cả 3 kim loại đều đứng sau Mg trong dãy điện hóa → Cả 3 kim loại đều không khử được ion Mg2+ trong muối.
→ Đáp án D
Câu 6: Cho khí CO dư đi qua hỗn hợp gồm CuO, Al2O3 và MgO (nung nóng). Khi phản ứng xảy ra hoàn toàn thu được chất rắn gồm :
A. Cu, Al, Mg. B. Cu, Al, MgO.
C. Cu, Al2O3, Mg. D. Cu, Al2O3, MgO.
Lời giải:
CO khử được các oxit kim loại của kim loại đứng sau Al trong dãy điện hóa thành kim loại và khí CO2.
→ CO chỉ khử được CuO thành Cu; Al2O3 và MgO không bị khử.
→ Đáp án D
Câu 7: Nguyên tử kim loại khi tham gia phản ứng hoá học có tính chất nào sau đây ?
A. Nhường electron và tạo thành ion âm.
B. Nhường electron và tạo thành ion dương.
C. Nhận electron để trở thành ion âm.
D. Nhận electron để trở thành ion dương.
Lời giải:
Nguyên tử kim loại khi tham gia phản ứng hóa học đóng vai trò chất khử → Nhường electron và tạo thành ion dương.
→ Đáp án B
Câu 8: Cặp chất không xảy ra phản ứng là
A. Fe + Cu(NO3)2. B. Cu + AgNO3.
C. Zn + Fe(NO3)2. D. Ag + Cu(NO3)2.
Lời giải:
Ag đứng sau Cu trong dãy điện hóa → Ag không thể khử ion Cu2+.
→ Đáp án D
Câu 9: Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo ra dung dịch có môi trường bazơ là:
A. Na, Ba, K. B. Be, Na, Ca.
C. Na, Fe, K. D. Na, Cr, K.
Lời giải:
Các kim loại phản ứng với nước ở điều kiện thường tạo ra dung dịch có môi trường bazơ là: Li, Na, K, Ca, Ba. → Chỉ đáp án A thỏa mãn.
→ Đáp án A
Câu 10: Để loại bỏ kim loại Cu ra khỏi hỗn hợp bột gồm Ag và Cu, người ta ngâm hỗn hợp kim loại trên vào lượng dư dung dịch
A. AgNO3. B. HNO3.
C. Cu(NO3)2. D. Fe(NO3)2.
Lời giải:
Ta ngâm vào lượng dư dung dịch AgNO3 vì Cu phản ứng với AgNO3 tạo thành dung dịch muối và đẩy kim loại Ag ra khỏi muối.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag.
→ Đáp án A
Câu 11: Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi
A. cấu tạo mạng tinh thể của kim loại.
B. khối lượng riêng của kim loại.
C. các electron độc thân trong tinh thể kim loại
D. các electron tự do trong tinh thể kim loại.
Lời giải:
Những tính chất vật lí chung của kim loại (dẫn điện, dẫn nhiệt, dẻo, ánh kim) gây nên chủ yếu bởi các e tự do trong tinh thể kim loại.
→ Đáp án D
Câu 12: So với nguyên tử phi kim cùng chu kì, nguyên tử kim loại
A. thường có bán kính nguyên tử nhỏ hơn.
B. thường có năng lượng ion hoá nhỏ hơn.
C. thường dễ nhận electron trong các phản ứng hoá học.
D. thường có số electron ở các phân lớp ngoài cùng nhiều hơn.
Lời giải:
So với nguyên tử phi kim cùng chu kì, nguyên tử kim loại thường có năng lượng ion hóa nhỏ hơn.
→ Đáp án B
Câu 13: Kim loại nào sau đây có tính dẫn điện tốt nhất trong tất cả các kim loại ?
A. Vàng B. Bạc
C. Đồng D. Nhôm
Lời giải:
Kim loại dẫn điện tốt nhất là bạc (Ag).
→ Đáp án B
Câu 14: Kim loại nào sau đây dẻo nhất trong tất cả các kim loại ?
A. Vàng B. Bạc
C. Đồng D. Nhôm
Lời giải:
Kim loại dẻo nhất trong tất cả các kim loại là vàng (Au).
→ Đáp án A
Câu 15: Kim loại nào sau đây có độ cứng lớn nhất trong tất cả các kim loại ?
A. Vonfam B. Crom
C. Sắt D. Đồng
Lời giải:
Kim loại có độ cứng lớn nhất trong tất cả các kim loại là crom (Cr).
→ Đáp án B
Câu 16: Kim loại nào sau đây là kim loại mềm nhất trong tất cả các kim loại ?
A. Liti B. Xesi
C. Natri D. Kalim
Lời giải:
Kim loại mềm nhất trong tất cả các kim loại là Xesi (Xe).
→ Đáp án B
Câu 17: Kim loại có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại ?
A. Vonfam B. Đồng
C. Sắt D. Kẽm
Lời giải:
Kim loại có nhiệt độ nóng chảy cao nhất trong tất cả các kim loại Vonfam.
→ Đáp án A
Câu 18: Kim loại nào sau đây nhẹ nhất (có khối lượng riêng nhỏ nhất) trong tất cả các kim loại
A. Liti B. Rubidi
C. Natri D. Kali
Lời giải:
Kim loại nhẹ nhất (khối lượng riêng nhỏ nhất) trong tất cả các kim loại là Li (D = 0,5g/cm3).
→ Đáp án A
Câu 19: Bao nhiêu gam clo tác dụng vừa đủ kim loại nhôm tạo ra 26,7 gam AlCl3?
A. 21,3 gam B. 12,3 gam.
C. 13,2 gam. D. 23,1 gam.
Lời giải:
2Al + 3Cl2 → 2AlCl3
Theo bài ta có: nAlCl3 = 26,7/133,5 = 0,2 mol
Theo phương trình ta có: nCl2 = 3nAlCl3/2 = 0,3 mol
Khối lượng clo cần là: mCl2 = 0,3.71 = 21,3 g
→ Đáp án A
Câu 20: Một thanh kim loại M hóa trị 2 được nhúng vào trong 1 lít dung dịch CuSO4 0,5M. Sau khi lấy thanh M ra và cân lại ,thấy khối lượng thanh tăng 1,6 gam, nồng độ CuSO4 còn 0,3M. Hãy xác định kim loại M?
A. Fe B. Mg
C. Zn D. Pb
Lời giải:
M + Cu2+ → M2+ + Cu
Số mol Cu2+ phản ứng là: 1(0,5 – 0,3) = 0,2 mol
Độ tăng khối lượng của thanh kim loaị M:
M = mCu – mM tan = 0,2(64 – M) = 1,6
Suy ra: M = 56 là Fe
→ Đáp án A
Câu 21: Ngâm một lá kẽm trong 100ml dung dịch AgNO3 0,1 mol. Kết thúc phản ứng, khối lượng lá kẽm là bao nhiêu?
A. 0,655g B. 0,75g
C. 0,65g D. 0,755g
Lời giải:
Ta có: nAgNO3 = 0,01 mol.
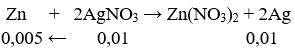
mAg = 0,01. 108 = 1,08g.
Đặt mZn = a ⇒ a = 1,08 – (0,005.65) = 0,755g.
→ Đáp án D
Câu 22: Cho 8,4 g Fe vào dung dịch có chứa 0,4mol AgNO3. Kết thúc phản ứng, khối lượng bạc là bao nhiêu?
A. 42,3g B. 23,4g
C. 43,2g D. 21,6g
Lời giải:
Ta có: nFe = 0,15 mol, nAgNO3 = 0,4mol.
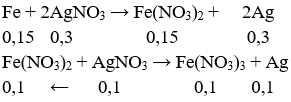
Suy ra: mAg = (0,1+ 0,3).108 = 43,2g.
→ Đáp án C
Câu 23: Cho biết các cặp oxi hoá - khử sau: Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+
Tính oxi hoá tăng dần theo thứ tự
A. Cu2+, Fe2+, Fe3+ B. Cu2+, Fe3+,Fe2+
C. Fe3+,Cu2+, Fe2+ D. Fe2+ ,Cu2+, Fe3+
Lời giải:
Tính oxi hoá tăng dần từ trái sang phải: Fe2+ ,Cu2+, Fe3+.
→ Đáp án D
Câu 24: Muốn khử dd chứa Fe3+ thành dd có chứa Fe2+ cần dùng kim loại sau:
A. Cu B. Na
C. Zn D. Ag
Lời giải:
2Fe3+ + Cu → Cu2+ + 2Fe2+
→ Đáp án A
Câu 25: Cho các kim loại: Fe , Al , Mg , Cu , Zn , Ag. Số kim loại tác dụng được với dd H2SO4 loãng là:
A. 5 B. 3
C. 6 D. 4
Lời giải:
Kim loại đứng trước H trong dãy điện hoá tác dụng được với dung dịch axit H2SO4 loãng: Fe, Al, Mg, Zn.
→ Đáp án D
Câu 26: Ngâm Cu dư vào dd AgNO3 thu được dd X, sau đó ngâm Fe dư vào dung dịch X thu được dung dịch Y. dung dịch Y gồm:
A. Fe(NO3)2 B. Fe(NO3)2 , Cu(NO3)2 , AgNO3
C. Fe(NO3)2 , Cu(NO3)2 D. Fe(NO3)3
Lời giải:
Ngâm Cu dư vào dd AgNO3, Ag bị đẩy hết ra khỏi muối, muối mới là Cu(NO3)2 (dd X).
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Ngâm Fe dư vào dung dịch X, Cu bị đẩy hết ra khỏi muối tạo muối mới là Fe(NO3)2.
Fe + Cu(NO3)2 → Fe(NO3)2 + Cu
→ Đáp án A
Câu 27: Ngâm đinh sắt sạch trong 200 ml dd CuSO4. Sau phản ứng kết thúc lấy đinh sắt ra rửa nhẹ và làm khô thấy khối lượng đinh sắt tăng 8 gam. Nồng độ CuSO4 ban đầu là:
A. 0,52 M B. 0,5 M
C. 5 M D. 0,25 M
Lời giải:
Gọi số mol Fe phản ứng là x mol.
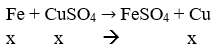
→ mtăng = 64x – 56x = 8 → x = 1 mol
→ nCuSO4 = x = 1 mol → CM(CuSO4) = 1/0,2 = 5M
→ Đáp án C
Câu 28: Cho 4 dung dịch muối: CuSO4, K2SO4, NaCl, KNO3. Dung dịch nào sau khi điện phân cho ra một dung dịch axit (điện cực trơ)
A. CuSO4 B. K2SO4
C. NaCl D. KNO3
Lời giải:
2NaCl + 2H2O -Dp→ 2NaOH + Cl2 + H2
CuSO4 + H2O -Dp→ Cu + H2SO4 + 0,5O2
Điện phân dung dịch KNO3 và K2SO4 thực chất là quá trình điện phân nước
2H2O -Dp→ 2H2 + O2.
→ Đáp án A
Câu 29: Cho các kim loại sau: K, Ba, Cu và Ag. Số kim loại điều chế được bằng phương pháp điện phân dung dịch (điện cực trơ) là:
A. 3 B. 1
C. 2 D. 4
Lời giải:
Điện phân dung dịch dùng để điều chế những kim loại trung bình hoặc yếu như Cu, Ag.
→ Đáp án C
Bài 30: Trong công nghiệp, kim loại nào sau đây được điều chế bằng phương pháp điện phân nóng chảy?
A. Fe B. Cu
C. Mg D. Ag
Lời giải:
Phương pháp điện phân nóng chảy dùng để điều chế các kim loại từ nhôm trở về trước.
VD: K, Na, Mg…
→ Đáp án C
Câu 31: Trong quá trình điện phân, các muối X- (X: Cl-, Br-) di chuyển về:
A. Cực dương và bị oxi hóa B. Cực âm và bị oxi hóa
C. Cực dương và bị khử D. Cực âm và bị khử
Lời giải:
Ion âm bị hút về cực dương (hay di chuyển về cực dương) và bị khử: 2X- + 2e → X2
→ Đáp án C
Câu 32: Cho dung dịch chứa các ion: Na+, K+, Cu+, Cl-, SO42-, NO32-. Các ion nào không bị điện phân khi ở trạng thái dung dịch:
A. Na+, K+, Cl-, SO42-
B. K+, Cu+, Cl-, NO32-
C. Na+, Cu+, Cl-, SO42-
D. Na+, K+, SO42-, NO32-
Lời giải:
Ion của kim loại mạnh như: K, Na, Li, Ca… và ion của các gốc muối có oxi như: SO42-, NO3- không bị điện phân. → Chọn D.
→ Đáp án D
Câu 33: Điện phân một lượng dư dung dịch MgCl2 (điện cực trơ, có màng ngăn xốp bao điện cực) với cường độ dòng điện 2,68A trong 2 giờ. Sau khi dừng điện phân khối lượng dung dịch giảm m gam, giả thiết nước không bay hơi, các chất tách ra đều khan. Giá trị của m là:
A. 8,7 B. 18,9
C. 7,3 D. 13,1.
Lời giải:
Phản ứng: MgCl2 + 2H2O -đpdd Mg(OH)2 + H2 + Cl2
- Ta có: ne trao đổi = It/F = 0,2 mol
→ nMgCl2 = nCl2 = nH2 = ne/2 = 0,1 mol
→ mdd giảm = 58nMg(OH)2 + 2nH2 + 71nCl2 = 13,1 gam
→ Đáp án D
Câu 34: Điện phân nóng chảy hoàn toàn 1,9g muối clorua của kim loại M được 0,48g kim loại M ở catot. Kim loại M là:
A. Zn B. Ca
C. Mg D. Ba
Lời giải:
Gọi muối cần tìm là MCln.
Bảo toàn khối lượng ta có:
mCl2 = mMCln - mM = 1,9 - 0,48 = 1,42 gam → nCl2 = 1,42/71 = 0,02 mol
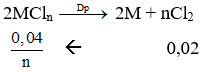
Theo bài ta có:
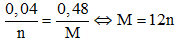
Vậy M là Mg.
→ Đáp án C
Câu 35: Điện phân một dd muối MCln với điện cực trơ. Khi ở catot thu được 16g kim loại M thì ở anot thu được 5,6 lít khí (đktc). Kim loại M là:
A. Mg B. Fe
C. Cu D. Ca
Lời giải:
nM = 16/M mol; nCl2 = 5,6/22,4 = 0,25 mol
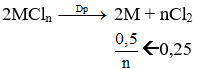
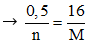
Kim loại M là Cu.
→ Đáp án C
Câu 36: Nếu muốn điện phân hoàn toàn (mất màu xanh) 400 ml dung dịch CuSO4 0,5M với cường độ dòng điện I = 1,34A (hiệu suất điện phân là 100%) thì cần bao nhiêu thời gian.
A. 6 giờ B. 7 giờ
C. 8 giờ D. 9 giờ
Lời giải:
nCuSO4 = 0,5. 0,4 = 0,2 mol
ne trao đổi = 2.0,2 = 0,4 mol
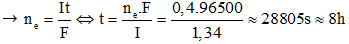
→ Đáp án C
Câu 37: Điện phân dung dịch muối CuSO4 dư trong thời gian 1930 giây, thu được 1,92 gam Cu ở catot. Cường độ dòng điện trong quá trình điện phân là giá trị nào dưới đây:
A. 3A B. 4,5A
C. 1,5A D. 6A
Lời giải:
Ta có:
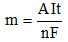
Với F = 96500 C/mol ta có:
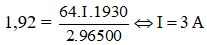
→ Đáp án A
Câu 38: Điện phân hòa toàn 2,22 gam muối clorua kim loại ở trạng thái nóng chảy thu được 448 ml khí (ở đktc) ở anot. Kim loại trong muối là:
A. Na B. Ca
C. K D. Mg
Lời giải:
nCl2 = 0,02 mol
Tại catot: Mn+ + ne → M
Theo định luật bảo toàn khối lượng mM = m(muối) – mCl2 = 2,22 – 0,02.71 = 0,8 gam
Tại anot: 2Cl- → Cl2 + 2e
Theo định luật bảo toàn mol electron ta có: nM = 0,04/n → M = 20.n → n = 2 và M là Ca
→ Đáp án B
Câu 39: Điện phân 250g dd CuSO4 8% đến khi nồng độ CuSO4 trong dd thu được giảm đi và bằng một nửa so với trước phản ứng thì dừng lại. Khối lượng kim bám ở catot gần với giá trị nào?
A. 4,08g B. 2,04g
C. 4,58g D. 4,5g
Lời giải:
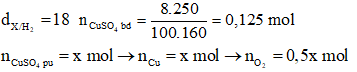
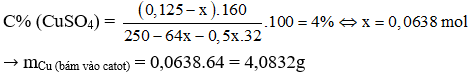
→ Đáp án A
Câu 40: Điện phân dung dịch CuCl2, điện cực trơ bằng dòng điện 5A trong 45 phút 20 giây. Tính khối lượng kim loại sinh ra ở Catot và V lít (đktc) khí sinh ra ở Anot.
A. 4,512g B. 4,5g
C. 4,6g D. 4,679g
Lời giải:
Phương trình điện phân:
CuCl2 -đpdd→ Cu + Cl2↑
Áp dụng công thức Faraday:
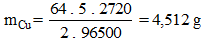
→ Đáp án A
Câu 41: (Đại học khối A - 2008) Biết rằng ion Pb2+ trong dung dịch oxi hóa được Sn. Khi nhúng hai thanh kim loại Pb và Sn được nối với nhau bằng dây dẫn điện vào một dung dịch chất điện li thì
A. Cả Pb và Sn đều bị ăn mòn điện hóa.
B. Cả Pb và Sn đều không bị ăn mòn điện hóa.
C. Chỉ có Pb bị ăn mòn điện hóa.
D. Chỉ có Sn bị ăn mòn điện hóa.
Lời giải:
Chỉ có Sn bị ăn mòn điện hóa
→ Đáp án D
Câu 42: (Trường THPT Lý Thái Tổ - 2014) Có 4 dung dịch riêng biệt: CuSO4, ZnCl2, FeCl3, AgNO3. Nhúng vào mỗi dung dịch một thanh Ni. Số trường hợp xuất hiện ăn mòn điện hoá là
A. 2 B. 3
C. 4 D. 1
Lời giải:
CuSO4 + Ni → ăn mòn điện hóa
ZnCl2 + Ni → không ăn mòn điện hoá
FeCl3 + Ni → không ăn mòn điện hoá
AgNO3 + Ni → ăn mòn điện hóa
→ Đáp án A
Câu 43: (Trường THPT Đức Hòa - Long An - 2015) Trường hợp nào dưới đây, kim loại không bị ăn mòn điện hóa?
A. Đốt Al trong khí Cl2.
B. Để gang ở ngoài không khí ẩm.
C. Vỏ tàu làm bằng thép neo đậu ngoài bờ biển
D. Fe và Cu tiếp xúc trực tiếp cho vào dung dịch HCl.
Lời giải:
Đốt Al trong khí Cl2; ăn mòn hóa học
Để gang ở ngoài không khí ẩm; ăn mòn điện hóa
Vỏ tàu làm bằng thép neo đậu ngoài bờ biển; ăn mòn điện hóa
Fe và Cu tiếp xúc trực tiếp cho vào dung dịch HCl; ăn mòn điện hóa
→ Đáp án A
Câu 44: (Trường THPT Trí Đức - Hà Nội - 2015) Tiến hành các thí nghiệm sau:
(a) Cho lá Fe vào dung dịch gồm CuSO4 và H2SO4 loãng;
(b) Đốt dây Fe trong bình đựng khí O2;
(c) Cho lá Cu vào dung dịch gồm Fe(NO3)3 và HNO3;
(d) Cho lá Zn vào dung dịch HCl;
Số thí nghiệm có xảy ra ăn mòn điện hóa là
A. 3 B. 2
C. 1 D. 4
Lời giải:
(a) Cho lá Fe vào dung dịch gồm CuSO4 và H2SO4 loãng; ăn mòn điện hóa
(b) Đốt dây Fe trong bình đựng khí O2; ăn mòn hóa học
(c) Cho lá Cu vào dung dịch gồm Fe(NO3)3 và HNO3; ăn mòn hóa học
(d) Cho lá Zn vào dung dịch HCl; ăn mòn hóa học
→ Đáp án C
Câu 45: (Cao đẳng khối A - 2013): Phát biểu nào dưới đây không đúng?
A. Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại.
B. Bản chất của ăn mòn kim loại là quá trình oxi hóa - khử.
C. Tính chất hóa học đặc trưng của kim loại là tính khử.
D. Ăn mòn hóa học phát sinh dòng điện.
Lời giải:
Nguyên tắc chung để điều chế kim loại là khử ion kim loại thành nguyên tử kim loại. Đúng
Bản chất của ăn mòn kim loại là quá trình oxi hóa - khử. Đúng
Tính chất hóa học đặc trưng của kim loại là tính khử. Đúng
Ăn mòn hóa học phát sinh dòng điện. Sai
→ Đáp án D
Câu 46: Tiến hành các thí nghiệm sau:
a. Cho lá Zn vào dung dịch gồm CuSO4 và H2SO4 loãng;
b. Đốt dây Cu trong bình đựng khí O2;
c. Cho lá Cu vào dung dịch Fe(NO3)2;
d. Cho lá Fe vào dung dịch HCl;
Số thí nghiệm có xảy ra ăn mòn điện hóa là
A. 3 B. 2
C. 1 D. 4
Lời giải:
a. Cho lá Zn vào dung dịch gồm CuSO4 và H2SO4 loãng; ăn mòn điện hóa
b. Đốt dây Cu trong bình đựng khí O2; ăn mòn hóa học
c. Cho lá Cu vào dung dịch Fe(NO3)2; không phản ứng
d. Cho lá Fe vào dung dịch HCl; ăn mòn hóa học
→ Đáp án C
Câu 47: (Trường THPT Đinh Chương Dương - 2015) Trường hợp nào sau đây kim loại bị ăn mòn điện hoá học?
A. Cho kim loại Zn nguyên chất vào dung dịch HCl
B. Cho kim loại Cu nguyên chất vào trong dung dịch HNO3 loãng
C. Thép cacbon để trong không khí ẩm
D. Đốt dây sắt nguyên chất trong khí O2
Lời giải:
Cho kim loại Zn nguyên chất vào dung dịch HCl; ăn mòn hóa học
Cho kim loại Cu nguyên chất vào trong dung dịch HNO3 loãng; ăn mòn hóa học
Thép cacbon để trong không khí ẩm; ăn mòn điện hóa
Đốt dây sắt nguyên chất trong khí O2; ăn mòn hóa học
→ Đáp án C
Câu 48: (Trường THPT Hải Lăng - Quảng Trị - 2015) Khi vật bằng gang, thép bị ăn mòn điện hóa trong không khí ẩm, nhận định nào sau đây là nhận định đúng:
A. Tinh thể cacbon là cực âm xảy ra quá trình oxi hóa
B. Tinh thể cacbon là cực dương, xảy ra quá trình oxi hóa
C. Tinh thể sắt cực dương xảy ra quá trình khử
D. Tinh thể sắt là cực âm xảy ra quá trình oxi hóa
Lời giải:
Tinh thể sắt là cực âm xảy ra quá trình oxi hóa.
→ Đáp án D
Câu 49: (Trường THPT Chuyên Tuyên Quang - 2015) Tiến hành các thí nghiệm sau:
- Ngâm một lá đồng trong dung dịch AgNO3.
- Ngâm một lá kẽm trong dung dịch HCl loãng.
- Ngâm một lá nhôm trong dung dịch NaOH.
- Ngâm ngập một đinh sắt được quấn một đoạn dây đồng trong dung dịch NaCl.
- Để một vật bằng gang ngoài không khí ẩm.
- Ngâm một miếng đồng vào dung dịch Fe2(SO4)3.
Số thí nghiệm xảy ra ăn mòn điện hóa là
A. 4. B. 2
C. 3. D. 1.
Lời giải:
- Ngâm một lá đồng trong dung dịch AgNO3; ăn mòn điện hóa
- Ngâm một lá kẽm trong dung dịch HCl loãng; ăn mòn hóa học
- Ngâm một lá nhôm trong dung dịch NaOH; ăn mòn hóa học
- Ngâm ngập một đinh sắt được quấn một đoạn dây đồng trong dung dịch NaCl. ăn mòn điện hóa
- Để một vật bằng gang ngoài không khí ẩm; ăn mòn điện hóa
- Ngâm một miếng đồng vào dung dịch Fe2(SO4)3; ăn mòn hóa học
→ Đáp án C
Câu 50: (Trường THPT Lê Văn Hưu - 2014) Thực hiện các thí nghiệm sau:
(1) Thả một viên Fe vào dung dịch HCl.
(2) Thả một viên Fe vào dung dịch Cu(NO3)2.
(3) Thả một viên Fe vào dung dịch FeCl3.
(4) Nối một dây Ni với một dây Fe rồi để trong không khí ẩm.
(5) Đốt một dây Fe trong bình kín chứa đầy khí O2.
(6) Thả một viên Fe vào dung dịch chứa đồng thời CuSO4 và H2SO4 loãng.
Trong các thí nghiệm trên thì thí nghiệm mà Fe không bị ăn mòn điện hóa học là
A. (2), (3), (4), (6). B. (1), (3), (4), (5).
C. (2), (4), (6). D. (1), (3), (5).
Lời giải:
(1) Thả một viên Fe vào dung dịch HCl; ăn mòn hóa học
(2) Thả một viên Fe vào dung dịch Cu(NO3)2; ăn mòn điện hóa
(3) Thả một viên Fe vào dung dịch FeCl3; ăn mòn hóa học
(4) Nối một dây Ni với một dây Fe rồi để trong không khí ẩm; ăn mòn điện hóa
(5) Đốt một dây Fe trong bình kín chứa đầy khí O2; ăn mòn hóa học
(6) Thả một viên Fe vào dung dịch chứa đồng thời CuSO4 và H2SO4 loãng; ăn mòn điện hóa.
→ Đáp án D
Câu 51: (Trường THPT Chuyên Nguyễn Huệ - Lần 3 - 2015) Trường hợp nào sau đây, kim loại bị ăn mòn điện hóa học?
A. Đốt dây sắt trong khí oxi khô.
B. Kim loại sắt trong dung dịch HNO3 loãng.
C. Kim loại kẽm trong dung dịch HCl.
D. Thép cacbon để trong không khí ẩm.
Lời giải:
Đốt dây sắt trong khí oxi khô; ăn mòn hóa học
Kim loại sắt trong dung dịch HNO3 loãng; ăn mòn hóa học
Kim loại kẽm trong dung dịch HCl; ăn mòn hóa học
Thép cacbon để trong không khí ẩm; ăn mòn điện hóa
→ Đáp án D
Câu 52: (Trường THPT Chuyên Vinh - Lần 2 - 2015) Ngâm một lá Zn tinh khiết trong dung dịch HCl, sau đó thêm vài giọt dung dịch CuSO4 vào. Trong quá trình thí nghiệm trên
A. chỉ xảy ra hiện tượng ăn mòn điện hóa học.
B. lúc đầu xảy ra hiện tượng ăn mòn điện hóa học sau đó xảy ra thêm hiện tượng ăn mòn hóa học.
C. lúc đầu xảy ra hiện tượng ăn mòn hóa học sau đó xảy ra thêm hiện tượng ăn mòn điện hóa học.
D. Chỉ xảy ra hiện tượng ăn mòn hóa học.
Lời giải:
Lúc đầu xảy ra hiện tượng ăn mòn hóa học sau đó xảy ra thêm hiện tượng ăn mòn điện hóa học.
→ Đáp án C
Câu 53: (Trường THPT Chuyên Vinh - Lần 2 - 2015) Tiến hành các thí nghiệm sau:
- TN 1: Cho hơi nước đi qua ống đựng bột sắt nung nóng.
- TN 2: Cho đinh sắt nguyên chất vào dung dịch H2SO4 loãng có nhỏ thêm vài giọt dung dịch CuSO4.
- TN 3: Cho từng giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3.
- TN 4: Để thanh thép (hợp kim của sắt với cacbon) trong không khí ẩm.
- TN 5: Nhúng lá kẽm nguyên chất vào dung dịch CuSO4.
Số trường hợp xảy ra ăn mòn điện hoá học là:
A. 3. B. 4.
C. 1. D. 2.
Lời giải:
- TN 1: Cho hơi nước đi qua ống đựng bột sắt nung nóng; ăn mòn hóa học
- TN 2: Cho đinh sắt nguyên chất vào dung dịch H2SO4 loãng có nhỏ thêm vài giọt dung dịch CuSO4; ăn mòn điện hóa
- TN 3: Cho từng giọt dung dịch Fe(NO3)2 vào dung dịch AgNO3; không phải ăn mòn kim loại
- TN 4: Để thanh thép (hợp kim của sắt với cacbon) trong không khí ẩm; ăn mòn điện hóa
- TN 5: Nhúng lá kẽm nguyên chất vào dung dịch CuSO4. ăn mòn điện hóa
→ Đáp án A
Câu 54: (Trường THPT Diễn Châu 5 - 2015) Nếu vật làm bằng hợp kim Fe-Zn bị ăn mòn điện hoá thì trong quá trình ăn mòn
A. sắt đóng vai trò anot và bị oxi hoá.
B. kẽm đóng vai trò anot và bị oxi hoá.
C. sắt đóng vai trò catot và ion H+ bị oxi hóa.
D. kẽm đóng vai trò catot và bị oxi hóa.
Lời giải:
Kẽm đóng vai trò anot và bị oxi hoá.
→ Đáp án B
Câu 55: (Trường THPT Nguyễn Thông - Vĩnh Long - 2015) Trường hợp nào sau đây xảy ra ăn mòn điện hoá?
A. Sợi dây bạc nhúng trong dung dịch HNO3.
B. Đốt lá sắt trong khí Cl2.
C. Thanh nhômnhúng trong dung dịch H2SO4 loãng.
D. Thanh kẽm nhúng trong dung dịch CuSO4.
Lời giải:
Sợi dây bạc nhúng trong dung dịch HNO3; ăn mòn hóa học
Đốt lá sắt trong khí Cl2; ăn mòn hóa học
Thanh nhôm nhúng trong dung dịch H2SO4 loãng; ăn mòn hóa học
Thanh kẽm nhúng trong dung dịch CuSO4; ăn mòn điện hóa
→ Đáp án D
Câu 56: (Trường THPT Yên Viên - Hà Nội - 2015) Tiến hành các thí nghiệm sau đây:
(a) Ngâm một lá kẽm vào dung dịch CuSO4.
(b) Ngâm một lá đồng vào dung dịch FeCl3.
(c) Cho thép cacbon tiếp xúc với nước mưa.
(d) Cho thép vào dung dịch axit clohiđric.
(e) Để sắt tây tiếp xúc với nước tự nhiên.
Trong các thí nghiệm trên có bao nhiêu trường hợp xảy ra ăn mòn điện hóa?
A. 2. B. 5.
C. 3. D. 4.
Lời giải:
(a) Ngâm một lá kẽm vào dung dịch CuSO4; ăn mòn điện hóa
(b) Ngâm một lá đồng vào dung dịch FeCl3; ăn mòn hóa học
(c) Cho thép cacbon tiếp xúc với nước mưa; ăn mòn điện hóa
(d) Cho thép vào dung dịch axit clohiđric; ăn mòn điện hóa
(e) Để sắt tây tiếp xúc với nước tự nhiên; ăn mòn điện hóa
→ Đáp án D
Câu 57: Phương pháp thích hợp điều chế kim loại Mg từ MgCl2 là
A. điện phân dung dịch MgCl2.
B. điện phân MgCl2 nóng chảy.
C. nhiệt phân MgCl2.
D. dùng K khử Mg2+ trong dung dịch MgCl2.
Lời giải:
Các kim loại đứng trước Al, phương pháp điều chế thích hợp là điện phân nóng chảy hợp chất ion của chúng.
→ Đáp án B
Câu 58: Hai kim loại có thể điều chế bằng phương pháp nhiệt luyện là
A. Ca và Fe. B. Mg và Zn.
C. Na và Cu. D. Fe và Cu.
Lời giải:
Phương pháp nhiệt luyện để điều chế các kim loại hoạt động trung bình như Zn, Fe, Cu, Sn…
→ Đáp án D
Câu 59: “Ăn mòn kim loại” là sự phá huỷ kim loại do:
A. Tác dụng hoá học của môi trường xung quanh.
B. Kim loại tác dụng với dung dịch chất điện ly tạo nên dòng diện.
C. Kim loại phản ứng hoá học với chất khí hoặc hơi nước ở nhiệt độ cao.
D. Tác động cơ học.
Lời giải:
“Ăn mòn kim loại” là sự phá hủy kim loại do tác dụng hóa học của môi trường xung quanh.
→ Đáp án A
Câu 60: Để chống ăn mòn cho đường ống dẫn dầu bằng thép chôn dưới đất, người ta dùng phương pháp điện hoá. Trong thực tế, người ta dùng kim loại nào sau đây làm điện cực hi sinh?
A. Zn. B. Sn.
C. Cu. D. Na.
Lời giải:
Kim loại dùng làm điện có tính khử mạnh hơn sắt loại B, C và D vì Na có tính khử quá mạnh không thể dùng làm điện cực hi sinh.
→ Đáp án A
Câu 61: (Trường THPT Hà Nội - Amsterdam - 2015) Cho các cặp kim loại nguyên chất tiếp xúc trực tiếp với nhau: Fe và Pb; Fe và Zn; Fe và Sn; Fe và Ni. Khi nhúng các cặp kim loại trên vào dung dịch axit, số cặp kim loại trong đó Fe bị phá huỷ trước là
A. 1. B. 3.
C. 2. D. 4.
Lời giải:
Fe và Pb sắt bị phá hủy trước
Fe và Zn kẽm bị phá hủy trước
Fe và Sn sắt bị phá hủy trước
Fe và Ni sắt bị phá hủy trước
→ Đáp án B
Câu 62: (Trường THPT Lộc Ninh - 2015) Kim loại M bị ăn mòn điện hoá học khi tiếp xúc với sắt trong không khí ẩm. M có thể là
A. Bạc. B. Đồng.
C. Chì. D. Kẽm.
Lời giải:
Kim loại M bị ăn mòn điện hoá học khi tiếp xúc với sắt trong không khí ẩm M phải đứng trước sắt M: Zn
→ Đáp án D
Câu 63: (Sở Giáo dục và Đào tạo Vĩnh Phúc - 2014) Trường hợp xảy ra ăn mòn điện hóa là
A. Nhúng thanh Fe vào dung dịch chứa hỗn hợp H2SO4 loãng và lượng nhỏ CuSO4.
B. Nhúng thanh Fe vào dung dịch hỗn hợp Fe2(SO4)3 và H2SO4 loãng.
C. Nhúng thanh Fe vào dung dịch Fe2(SO4)3.
D. Nhúng thanh Fe vào dung dịch H2SO4 loãng.
Lời giải:
Nhúng thanh Fe vào dung dịch chứa hỗn hợp H2SO4 loãng và lượng nhỏ CuSO4; ăn mòn điện hóa
Nhúng thanh Fe vào dung dịch hỗn hợp Fe2(SO4)3 và H2SO4 loãng; ăn mòn hóa học
Nhúng thanh Fe vào dung dịch Fe2(SO4)3; ăn mòn hóa học
Nhúng thanh Fe vào dung dịch H2SO4 loãng; ăn mòn hóa học
→ Đáp án A
Câu 64: Kim loại nào sau đây có tính khử mạnh nhất?
A. Fe B. K
C. Mg D. Al.
Lời giải:
Từ trái sang phải trong dãy điện hóa tính khử kim loại giảm dần.
Thứ tự từ trái sang phải các kim loại trong các đáp án trong dãy điện hóa: K, Mg, Al, Fe.
→ Đáp án B
Câu 65: Cho các nửa phản ứng:
(1) Cu2+ + 2e → Cu;
(2) Cu → Cu2+ + 2e
(3) 2H2O + 2e → H2 + 2OH-;
(4) 2H2O → O2 + 4H+ + 4e
(5) 2Br- → Br2 + 2e;
(6) 2H+ + 2e → H2
Số nửa phản ứng xảy ra ở catot trong quá trình điện phân là:
A. 4 B. 5
C. 6 D. 3
Lời giải:
Ở catot trong quá trình điện phân là xảy ra quá trình khử (quá trình nhận e)
Số nửa phản ứng xảy ra ở catot trong quá trình điện phân là: 1, 3, 6.
→ Đáp án D.
Câu 66: Ở nhiệt độ cao, khí CO khử được các oxit nào sau đây:
A. Fe2O3 và CuO. B. Al2O3 và CuO.
C. MgO và Fe2O3. D. CaO và MgO.
Lời giải:
Khí CO chỉ khử được oxit của kim loại đứng sau Al trong dãy điện hóa. Chỉ đáp án A phù hợp.
→ Đáp án A
Câu 67: Điện phân dung dịch chứa HCl, NaCl, FeCl3 (điện cực trơ, có màng ngăn). Đồ thị nào sau đây biểu diễn đúng sự biến thiên pH của dung dịch theo thời gian (bỏ qua sự thuỷ phân của muối)?
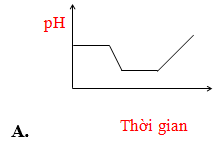
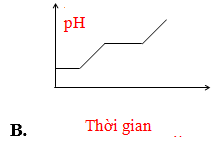
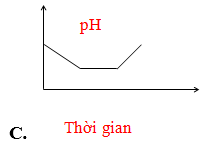
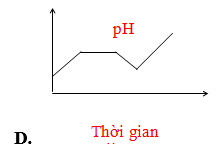
Lời giải:
Thứ tự:
Fe3+ + 1e → Fe2+ (pH không đổi)
H+ + 1e → 0,5H2 (pH tăng vì H+ bị điện phân)
Fe2+ + 2e → Fe (pH không đổi)
2H2O + 2e → 2OH- + H2 (pH tăng vì tạo OH).
→ Đáp án B
Câu 68: Cho 2,24 lit đktc khí CO đi từ từ qua một ống sứ nung nóng chứa m gam hỗn hợp MgO, Fe2O3, CuO. Sau phản ứng thu được (m - 0,8) gam chất rắn và hỗn hợp khí X. Tính tỷ khối hơi của X so với H2.
A. 14 B. 18
C. 12 D. 24
Lời giải:
Phản ứng tổng quát CO + Ooxit → CO2.
mran giam = mO pư = 0,8 g ⇒ nO pư = nCO2 = 0,05 mol
⇒ X gồm 0,05 mol CO và 0,05 mol CO2.
⇒ dX/H2 = 18
→ Đáp án B
Câu 69: Điện phân (điện cực trơ) dung dịch X chứa 0,2 mol CuSO4; 0,12 mol Fe2(SO4)3 và 0,44 mol NaCl bằng dòng điện có cường độ 2 ampe. Thể tích khí (đktc) thoát ra ở anoot sau 26055 giây điện phân là:
A. 5,936 lít B. 9,856 lít
C. 5,488 lit D. 4,928 lit.
Lời giải:
ne trao đổi = 2.26055:96500 = 0,54 mol
Tại anot:
+ 2Cl- → Cl2 + 2e
+ 2H2O → 4H+ + O2 + 4e
⇒ ne = nCl- + 4nO2 ⇒ nO2 = 0,025 mol
⇒ V = VCl2 + VO2 = 22,4.0,245 = 5,488 lít
→ Đáp án C
Câu 70: Cho Fe phản ứng với dd HNO3 đặc, nóng thu được một chất khí màu nâu đỏ. Chất khí đó là:
A. N2 B. NH3
C. NO2 D. N2O
Lời giải:
Khí màu nâu đỏ là NO2.
Fe + 6HNO3 → Fe(NO3)3 + 3NO2 + 3H2O
→ Đáp án C
Câu 71: Có thể dùng axit nào sau đây để hòa tan hoàn toàn hỗn hợp gồm: Al, Fe, Cu, Ag?
A. HCl
B. HNO3 loãng
C. H2SO4 loãng
D. H2SO4 đặc nguội.
Lời giải:
A, C sai: HCl và H2SO4 loãng không hòa tan được kim loại đứng sau H trong dãy hoạt động hóa học như Cu, Ag
D sai: H2SO4 đặc nguội không hòa tan được Al, Fe (Al, Fe bị thụ động hóa trong H2SO¬4 đặc nguội và HNO3 đặc nguội)
→ Đáp án B
Câu 72: Cho sơ đồ sau:
Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe → FeCl3.
Số phương trình phản ứng oxi hóa - khử trong dãy là:
A. 3 B. 4
C. 5 D. 6
Lời giải:
Những phản ứng có sự thay đổi số oxi hóa là phản ứng oxi hóa – khử (1,3,5,6)
(1) Fe + 2HCl → FeCl2 + H2
(2) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
(3) 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
(4) 2Fe(OH)3 -to→ Fe2O3 + 3H2O
(5) Fe2O3 + 2Al -to→ 2Fe + Al2O3
(6) Fe + Cl2 → FeCl3
→ Đáp án B
Câu 73: Phương trình phản ứng nào sau đây viết sai?
A. FeCO3 + 2HNO3 → Fe(NO3)2 + CO2 + H2O
B. 2FeCl2 + Cl2 → 2FeCl3
C. 2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2
D. Fe2O3 + 6HNO3 đặc -to→ 2Fe(NO3)3 + 3H2O.
Lời giải:
3FeCO3 + 10HNO3 → 3Fe(NO3)3 + 5H2O + NO + 3CO2
→ Đáp án A
Câu 74: Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng dư chất nào sau đây?
A. Mg B. Cu
C. Ba D. Na
Lời giải:
Cu + 2Fe3+ → Cu2+ + 2Fe2+
→ Đáp án B
Câu 75: Nguyên tử 23Z có cấu hình e là: 1s22s22p63s1. Z có
A. 11 nơtron, 12 proton.
B. 11 proton, 12 nơtron.
C. 13 proton, 10 nơtron.
D. 11 proton, 12 electron.
Lời giải:
Nguyên tử Z có số khối A = 23, số proton = số electron = 11
→ Số nơtron = A - Z = 23 - 11 = 12
→ Đáp án B
Câu 76: Cho sơ đồ chuyển hóa sau:
CaO -+X→ CaCl2 -+Y→ Ca(NO3)2 -+Z→ CaCO3
Công thức của X, Y, Z lần lượt là:
A. Cl2, AgNO3, MgCO3.
B. Cl2, HNO3, CO2.
C. HCl, HNO3, NaNO3.
D. HCl, AgNO3, (NH4)2CO3.
Lời giải:
- Đáp án A: Cl2, AgNO3, MgCO3: không xảy ra.
- Đáp án B: Cl2, HNO3, CO2: không xảy ra.
- Đáp án C: CaO + 2HCl → CaCl2 + H2O
CaCl2 + HNO3: không xảy ra
- Đáp án D: CaO + 2HCl → CaCl2 + H2O
CaCl2 + 2AgNO3 → Ca(NO3)2 + 2AgCl
Ca(NO3)2 + (NH4)2CO3 → CaCO3↓ + 2NH4NO3
→ Đáp án D
Câu 77: Cho sơ đồ sau: FeS2 → X → Y → Z → Fe
Các chất X, Y, Z lần lượt là:
A. FeS, Fe2O3, FeO.
B. Fe3O4, Fe2O3, FeO.
C. Fe2O3, Fe3O4, FeO.
D. FeO, Fe3O4, Fe2O3.
Lời giải:
2FeS2 + 11/2 O2 -to→ Fe2O3 + 4SO2
3Fe2O3 + CO -to→ 2Fe3O4 + CO2
Fe3O4 + CO -to→ 3FeO + CO2
FeO + CO -to→ Fe + CO2
→ Đáp án C
Câu 78: Có thể dùng dung dịch muối nào sau đây để hòa tan hoàn toàn hỗn hợp gồm: Al, Fe, Pb, Cu?
A. Cu(NO3)2 B. Pb(NO3)2
C. AgNO3 D. Al(NO3)3
Lời giải:
Kim loại mạnh đẩy kim loại yếu ra khỏi dung dịch muối của chúng
Nên chọn muối của KL yếu nhất là AgNO3
→ Đáp án C
Câu 79: Chất nào sau đây có thể oxi hóa Zn thành Zn2+?
A. Fe B. Ag+
C. Al3+ D. Ca2+
Lời giải:
Zn + 2Ag+ → Zn2+ + 2Ag (KL mạnh đẩy KL yếu ra khỏi dung dịch muối)
→ Đáp án B
Câu 80: Nung nóng từng cặp chất sau trong bình kín:
(1) H2(k) + CuO(r);
(2) C(r) + KClO3;
(3) Fe(r) + O2 (r)
(4) Mg(r) + SO2(k);
(5) Cl2 (k) + O2(k);
(6) K2O (r) + CO2(k)
Số trường hợp có phản ứng hóa học xảy ra là:
A. 4 B. 2
C. 3 D. 5
Lời giải:
(1) H2 + CuO → H2O + Cu
(2) 3C + 2KClO3 → 3CO2 + 2KCl
(3) 3Fe + 2O2 → Fe3O4
(4) 2Mg + SO2 → 2MgO + S
(6) K2O + CO2 → K2CO3
→ Đáp án D

