40 câu trắc nghiệm Phân biệt một số chất vô cơ có lời giải chi tiết (nâng cao) - Hoá học lớp 12
40 câu trắc nghiệm Phân biệt một số chất vô cơ có lời giải chi tiết (nâng cao)
Với 40 câu trắc nghiệm Phân biệt một số chất vô cơ có lời giải chi tiết (nâng cao) Hoá học lớp 12 tổng hợp 40 bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Phân biệt một số chất vô cơ từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

Câu 1. Cho ba dung dịch đựng trong ba lọ riêng biệt: CuSO4, Cr2(SO4)3 và FeSO4. Thuốc thử nào sau đây có thể phân biệt được cả ba lọ hóa chất trên?
A. HCl B. H2SO4
C.NaOH D. Ba(OH)2
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch NaOH lần lượt vào các mẩu thử.
- Mẩu thử tạo kết tủa màu xanh là CuSO4.
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
- Mẩu thử tạo kết tủa trắng xanh, sau đó hóa nâu đỏ là FeSO4.
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
- Mẩu thử tạo kết tủa xanh rêu, sau đó tan trong kiềm dư là Cr2(SO4)3.
Cr2(SO4)3 + 6NaOH → 2Cr(OH)3 + 3Na2SO4
Cr(OH)3 + NaOH → Na[Cr(OH)4]
→ Đáp án C
Câu 2. Có 5 dung dịch riêng rẽ, mỗi dung dịch chứa một cation: NH4+, Mg2+, Fe3+, Al3+, Na+ có nồng độ khoảng 0,1M. Nếu dùng dung dịch NaOH thì có thể nhận biết được mấy dung dịch?
A. 3 B. 4
C. 5 D. 2
Lời giải:
Các phản ứng xảy ra:
NH4+ + OH- → NH3↑ + H2O
Mg2+ + 2OH- → Mg(OH)2↓ tủa trắng
Fe3+ + 3OH- → Fe(OH)3↓ nâu đỏ
Al3+ + 3OH- → Al(OH)3
Al(OH)3 + 3 OH- → [Al(OH)4]- tan
Nhận biết được 4 dung dịch.
→ Đáp án B
Câu 3. Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dug dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH =2 ?
A. 36,5 ml B. 73ml
C. 22,4ml C. 300ml
Lời giải:
nNaOH = nOH = 0,25.V (mol)
nH+ = nHCl + 2nH2SO4 = 0,05. 0,1 + 0,05. 2. 0,05
pH = 2 → [H+] = 10-2 M = 0,01 mol
Ta có: (0,01 - 0,25V)/(0,05 + V) = 10-2
0,01 - 0,25.V = 0,01. 0,05 + 0,01 V → 0,26.V = 0,01 - 0,01.0,05
V = 0,0365 l = 36,5 ml
→ Đáp án A
Câu 4. Có thể phân biệt ba dung dịch loãng gồm KOH, HCl và H2SO4 bằng một thuốc thử là:
A. BaCO3 B. Quỳ tím
C. Al D. Zn
Lời giải:
Dùng BaCO3:
- Mẩu thử chỉ tạo khí là HCl.
2HCl + BaCO3 → BaCl2 + CO2 + H2O
- Mẩu thử vừa có khí vừa có kết tủa trắng là H2SO4.
H2SO4 + BaCO3 → BaSO4 + CO2 + H2
- Mẩu thử còn lại là KOH.
→ Đáp án A
Câu 5. Trong nước tự nhiên thường có lẫn những lượng nhỏ các muối Ca(NO3)2, Mg(NO3)2, Ca(HCO3)2 và Mg(HCO3)2. Có thể dùng một hóa chất nào sau đây để loại được tất cả các muối trên?
A. NaOH B. Na2CO3
C. NaHCO3 D. K2SO4
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch NaOH lần lượt vào các mẩu thử.
- Mẩu thử tạo kết tủa xanh là Cu(NO3)2.
Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
- Mẩu thử tạo kết tủa nâu đỏ là FeCl3.
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
- Mẩu thử tạo kết tủa keo trắng tan trong kiềm dư là A1C13.
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Al(OH)3 + NaOH → Na[Al(OH)4]
- Mẩu thử có khí mùi bay ra là NH4Cl.
NH4Cl + NaOH → NaCl + NH3 + H2O
→ Đáp án A
Câu 6. Lấy 25ml dung dịch A gồm FeSO4 và Fe2(SO4)3 rồi chuẩn độ bằng dung dịch hỗn hợp KMnO4 0,025M thì hết 18,10ml. Mặt khác, thêm lượng dư dung dịch NH3 vào 25ml dung dịch A thì thu được kết tủa, lọc kết tủa rồi nung đỏ trong không khí ở nhiệt độ cao đến khối lượng không đổi, cân được 1,2g. Nồng độ mol/l của FeSO4 và Fe2(SO4)3 lần lượt là:
A. 0,091 và 0,25 B. 0,091 và 0,265
C. 0,091 và 0,255 D. 0,087 và 0,255
Lời giải:
Ta có:
nFeSO4 = 5. nKMnO4 = 2,2615.10-3 mol
CM FeSO4 = 2,2625/0,025 = 0,091M
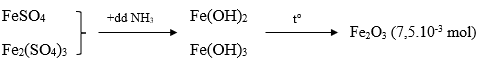
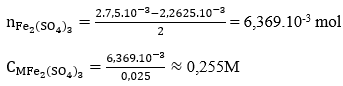
→ Đáp án C
Câu 7. Có ba chất rắn Zn(OH)2, Ni(OH)2, Cu(OH)2. Có thể dùng dung dịch nào để hòa tan được cả ba chất trên?
A. Dung dịch NaOH. B. Dung dịch NH3.
C. Dung dịch NH4Cl. D. Dung dịch KOH.
Lời giải:
Các hiđroxit này đều tan trong dung dịch NH3 dư do tạo phức.
Zn(OH)2 + 4NH3 → [Zn(NH3)4]2+ + 2OH-
Cu(OH)2 + 4NH3 → [Cu(NH3)4]2+ + 2OH-
Ni(OH)2 + 6NH3 → [Ni(NH3)6]2+ + 2OH-
→ Đáp án B
Câu 8. Có 5 dung dịch, mỗi dung dịch nồng đọ khoảng 0,1M của một trong các muối sau: KCl, Ba(HCO3)2, K2CO3, K2S, K2SO4. Chỉ dùng dung dịch H2SO4 loãng nhỏ trực tiếp vào từng dung dịch thì có thể nhận biết được dung dịch nào?
A. Hai dung dịch: Ba(HCO3)2, K2S.
B. Hai dung dịch: Ba(HCO3)2, K2CO3.
C. Hai dung dịch: Ba(HCO3)2, K2SO4.
D. Ba dung dịch: Ba(HCO3)2, K2CO3, K2S.
Lời giải:
H2SO4 + Ba(HCO3)2 → BaSO4 (trắng) + 2CO2↑ + 2H2O
H2SO4 + K2CO3 → K2SO4 + CO2↑ + H2O
H2SO4 + K2S → K2SO4 + H2S↑ (mùi trứng thối)
Nhận biết được 3 chất.
→ Đáp án D
Câu 9. Cho 5 lọ mất nhãn đựng các dung dịch: KNO3, Cu(NO3)2, FeCl3 và NH4Cl. Chỉ sử dụng duy nhất một thuốc thử, hãy nhận biết các dung dịch trên
A. HCl B. H2SO4
C. NaOH D. NH4+
Lời giải:
Trích mẫu thử cho mỗi lần thí nghiệm. cho dung dịch NaOH lần lượt vào các mẫu thử.
Mẫu thử tạo kết tủa xanh là Cu(NO3)2
Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
Mẫu thử tạo kết tủa nâu đỏ là FeCl3
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
Mẫu thử tạo kết tủa keo trắng tan trong kiềm dư là AlCl3
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Al(OH)3 + NaOH → Na[Al(OH)4]
Mẫu thử có khí mùi khai bay ra là NH4Cl
NH4Cl + NaOH → NaCl + NH3 + H2O
→ Đáp án C
Câu 10. Để xác định nồng đội dung dịch NaOH người ta tiến hành như sau: cân 1,26 gam axit oxalic ngậm nước (H2C2O4.2H2O) hòa tan hoàn toàn vào nước, định mức thành 100 ml. lấy 10 ml dung dịch này thêm vào đó vài giọt phenolphthalein, đem chuẩn độ bằng dung dịch NaOH đến xuất hiện màu hồng (ở pH = 9) thì hết 17,5 ml dung dịch NaOH. Tính nồng độ dung dịch NaOH đã dùng.
A. 0,114M B. 0,26M
C. 0,124M D. 0,16M
Lời giải:
Chuẩn độ: H2C2O4 + 2NaOH → Na2C2O4 + 2H2O
Nồng độ dung dịch H2C2O4: CH2C2O4 = (1,26/126). (1000/100) = 0,1M
Theo phản ứng: nNaOH = 2nH2C2O4. V = 2.10-3 mol ⇒ CM (NaOH) = 0,114M
→ Đáp án A
Câu 11. Cho ba dung dịch đựng trong ba lọ riêng biệt: CuSO4, Cr2(SO4)3 và FeSO4. Thuốc thử nào sau đây có thể phân biệt được cả ba lọ hóa chất trên?
A. HCl B. H2SO4
C. NaOH D. Ba(OH)2
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch NaOH lần lượt vào các mẩu thử.
- Mẩu thử tạo kết tủa màu xanh là CuSO4.
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
- Mẩu thử tạo kết tủa trắng xanh, sau đó hóa nâu đỏ là FeSO4.
FeSO4 + 2NaOH → Fe(OH)2 + Na2SO4
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
- Mẩu thử tạo kết tủa xanh rêu, sau đó tan trong kiềm dư là Cr2(SO4)3.
Cr2(SO4)3 + 6NaOH → 2Cr(OH)3 + 3Na2SO4
Cr(OH)3 + NaOH → Na[Cr(OH)4]
→ Đáp án C
Câu 12. Chuẩn độ 20 ml dung dịch hỗn hợp HCl 0,1M + HNO3 a mol/l cần dùng hết 16,5 ml dung dịch hỗn hợp KOH 0,1M và Ba(OH)2 0,05M. Giá trị của a là:
A. 0,07 B. 0,08
C. 0,065 D. 0,068
Lời giải:
∑nH+ = 0,02.0,1 + 0,02a
∑nOH- = 0,0165. 0,1 + 0,0165. 2. 0,05 = 3,3.10-3 mol
Trung hòa dung dịch thì ∑nH+ = ∑nOH-
0,02. 0,1 + 0,02a = 3,3.10-3 → a = 0,065 mol/l
→ Đáp án C
Câu 13. Chỉ dùng dung dịch HCl, hãy nên cách nhận biết các chất bột mà trắng sau: NaCl, BaCO3, Na2SO4, Na2S, BaSO4, MgCO3, ZnS.
A. BaSO4 B. NaOH
C. HCl D. H2O
Lời giải:
Trích mỗi chất một ít làm mẫu thử. Hòa tan các bột trên vào dung dịch HCl.
Không tan là BaSO4.
Tan nhanh và có múi trứng thối thoát ra là Na2S.
Na2S + 2HCl → 2NaCl + H2S (1)
Tan chậm và có mùi trứng thối thoát ra là H2S
ZnS + 2HCl → ZnCl2 + H2S (2)
Tan và sủi bọt khí không múi là BaCO3 và MgCO3
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (3)
MgCO3 + 2HCl → MgCl2 + CO2 + H2O (4)
Hai chất chỉ tan là NaCl và Na2SO4. Lấy từng dung dịch này đổ vào các dung dịch thu được ở (3) và (4) có kết tủa thì đó là dung dịch Na2SO4 và dung dịch BaCl2. Còn lại là dung dịch NaCl và MgCl2.
→ Đáp án C
Câu 14. Có 2 dung dịch riêng lẻ, chứa các anion NO3-, CO32-. Có thể dùng những hóa chất nào sau đây để nhận biêt được từng ion trong dung dịch đó?/
A. Dung dịch HCl và Cu.
B. Dung dịch HCl và CuO
C. Dung dịch HCl và Br2
D. Dung dịch HCl và dung dịch NaOH
Lời giải:
CO32- + 2H+ → CO2↑ + H2O
Nhận biết được CO32-
3Cu + 2 NO3- + 8H+ → 3Cu2+(màu xanh) + 2NO↑ + 4H2O
2NO + O2 → 2NO2 (nâu đỏ)
→ Đáp án A
Câu 15. Có bốn lọ hóa chất mất nhãn đựng riêng biệt bốn dung dịch muối CH3COONa, C6H5ONa, Na2CO3 và NaNO3. Thuốc thử nào sau đây c6 thể được dùng để phân biệt các muối trên?
A. NaOH B. H2SO4
C. HCl D. Cả B và C đều đúng
Lời giải:
Trích mẫu thử cho mỗi lần thí nghiệm. Cho dung dịch HCl lần lượt vào các mẫu thử.
- Mẫu nào có hiện tượng sủi bọt khí là Na2CO3.
Na2CO3 + 2HCl → 2NaCl + CO2 + H2O
- Mẫu nào bị vẩn đục khi lắc là C6H5ONa.
C6H5ONa + HCl → C6H5OH + NaCl
- Mẫu có mùi giấm bay ra là CH3COONa.
CH3COONa + HCl → CH3COOH + NaCl
- Mẫu không có hiện tượng gì là NaNO3.
→ Đáp án D
Câu 16. Cần thêm vào bao nhiêu ml dung dịch NaOH 0,25M vào 50 ml dug dịch hỗn hợp HCl 0,1M và H2SO4 0,05M để thu được dung dịch có pH = 2 ?
A. 35,5 ml B. 36,5 ml
C. 37,5 ml D. 38,5 ml
Lời giải:
nNaOH = nOH = 0,25.V (mol)
nH+ = nHCl + 2nH2SO4 = 0,05. 0,1 + 0,05. 2. 0,05
pH = 2 → [H+] = 10-2 M = 0,01 mol
Ta có: (0,01 - 0,25V)/(0,05 + V) = 10-2
⇒ 0,01 - 0,25.V = 0,01. 0,05 + 0,01 V → 0,26.V = 0,01 - 0,01. 0,05
⇒ V = 0,0365 l = 36,5 ml
→ Đáp án B
Câu 17. Để xác định nồng độ dung dịch H2O2, người ta hòa tan 0,5 gam nước oxi già vào nước, thêm H2SO4 tạo môi trường axit. Chuẩn độ dung dịch thu được cần vừa đủ 10 ml dung dịch KMnO4 0,1M. Xác định hàm lượng H2O2 trong nước oxi già.
A. 9% B. 17%
C. 12% D. 21%
Lời giải:
Phản ứng
5H2O2 + 2KMnO4 + 3H2SO4 → K2SO4 + 2MnSO4 + SO2 + 8H2O
Từ phản ứng ⇒ nH2O2 = 5/2 nKMnO4 = 2,5.10-3 (mol)
⇒
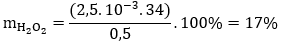
→ Đáp án B
Câu 18. Có 5 dung dịch mất nhãn gồm CuCl2, NaNO3, Mg(NO3)2; NH4NO3 và Fe(NO3)3. Có thể dùng kim loại nào sau đây để phân biệt cả 5 dung dịch?
A. Na B. Fe
C. Cu D. Ag
Lời giải:
Dùng Na
Na + H2O → NaOH + 1/2 H2
Sau đó:
CuCl2 + 2NaOH → Cu(OH)2↓ (xanh) + 2NaCl
Mg(NO3)2 + 2NaOH → Mg(OH)2↓ (trắng) + 2NaNO3
NH4NO3 + NaOH → NaNO3 + NH3↑ + H2O
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ (nâu đỏ) + 3NaNO3
→ Đáp án A
Câu 19. Hóa chất nào sau đây có thể nhận biết được đồng thời các dung dịch NaI, KCl và BaBr2 ?
A. Dung dịch AgNO3. B. Dung dịch HNO3.
C. Dung dịch NaOH. D. Dung dịch H2SO4.
Lời giải:
AgNO3 + NaI → AgI↓ (vàng) + NaNO3
AgNO3 + KCl → AgCl↓ (trắng) + KNO3
2AgNO3 + BaBr2 → 2AgBr↓ (vàng nhạt) + Ba(NO3)2
→ Đáp án A
Câu 20. Để xác định hàm lượng nitơ tổng trong chất hữu cơ, theo phương pháp Ken-đan người ta cân 2g mẫu rồi tiến hành vô cơ hóa mẫu để bộ lượng nitơ chuyển thành muối amoni. Sau đó sục dung dịch NaOH 40% vào dung dịch sau phản ứng. Lượng NH3 thoát ra được hấp thụ hoàn toàn bởi 20ml dung dịch H2SO4 0,1M.
Chuẩn độ lượng dư H2SO4 cần 10ml NaOH 0,1M nữa. Vậy %N trong chất hữu cơ là bao nhiêu?
A. 2,0% B. 2,2%
C. 1,8% D. 2,1%
Lời giải:
nH2SO4 = 0,02.0,1 = 0,002 mol; nNaOH = 0,01. 0,1 = 0,001 mol
NH4+ + OH- → NH3↑ + H2O
H2SO4 (0,0015) + 2NH3 (0,003) → (NH4)2SO4
H2SO4 (dư) (0,0005) + 2NaOH (0,001) → Na2SO4 + 2H2O
nNH3 = 0,003 mol → mN = 0,003. 14 = 0,042 (g)
%N = (0,042/2). 100% = 2,1%
→ Đáp án D
Câu 21. Có hai dung dịch (NH4)2S và (NH4)2SO4. Dùng dung dịch nào sau đây để nhận biết được cả hai dung dịch trên?
A. Dung dịch NaOH.
B. Dung dịch Ba(OH)2.
C. Dung dịch KOH.
D. Dung dịch HCl.
Lời giải:
Dùng Ba(OH)2
Có khí mùi khai là (NH4)2S
Có khí mùi khai và kết tủa trắng là (NH4)2SO4
(NH4)2S + Ba(OH)2 → BaS + 2NH3↑ + 2H2O
(NH4)2SO4 + Ba(OH)2 → BaSO4 + 2NH3↑ + 2H2O
→ Đáp án B
Câu 22. Cho ba hợp kim: Cu-Ag, Cu-Al, Cu-Zn. Thuốc thử nào sau đây có thể được dùng để phân biệt ba hợp kim trên?
A. HCl và NaOH
B. HNO3 và NH3
C. H2SO4 và NaOH
D. H2SO4 loãng và NH3
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch H2SO4 lần lượt vào các mẩu thử.
- Hợp kim nào không có khí là Cu-Ag.
- Cho dung dịch NH3 vào dung dịch thu được trong hai trường hợp còn lại.
+ Trường hợp tạo kết tủa keo trắng và không tan trong NH3 dư ⇒ hợp kim là Cu-Al.
3Al + 3H2SO4 → Al2(SO4)3 + 3H2
Al2(SO4)3 + 6NH3 + 6H2O → 2Al(OH)3 + 3(NH4)2SO4
+ Trường hợp tạo kết tủa rồi tan trong NH3 dư ⇒ hợp kim ban đầu là Cu-Zn.
Zn + H2SO4 → ZnSO4 + H2
ZnSO4 + 2NH3 + 2H2O → Zn(OH)2 + (NH4)2SO4
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2
→ Đáp án D
Câu 23. Có 3 ống nghiệm riêng rẽ, mỗi ống chứa một trong các ion sau: SO42-, SO32-, CO32-. Có thể dùng những hóa chất nào trong dãy sau đây để nhận biết từng ion?
A. Dung dịch Ca(OH)2.
B. Dung dịch HCl, dung dịch Br2 và BaCl2.
C. Dung dịch HCl, dung dịch Br2 và NaOH.
D. Dung dịch HCl, dung dịch Ca(OH)2.
Lời giải:
Trước hết cho HCl vào từng dung dịch
CO32- + 2H+ → CO2↑ + H2O
SO32- + 2H+ → SO2↑ + H2O
Nhận biết SO2 bằng dung dịch Br2
SO2 + Br2 + 2H2O → 2HBr + H2SO4
Nhận biết SO42- bằng dung dịch BaCl2
Ba2+ + SO42- → BaSO4↓
→ Đáp án B
Câu 24. Để xác định hàm lượng FeCO3 trong quặng xi đe rit, người ta làm như sau: còn 0,6g mẫu quặng, chế hóa nó theo một quy trình hợp lí, thu được FeSO4 trong môi trường H2SO4 loãng. Chuẩn đọ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2ml. % theo khối lượng của FeCO3 là:
A. 12,18% B. 24,26%
C. 60,9% D. 30,45%
Lời giải:
nKMnO4 = (0,025.25,2)/1000 = 6,3.10-4 mol
Phương trình phản ứng:
10FeSO4 (3,15.10-3) + 8H2SO4 + 2KMnO4 (6,3.10-4) → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
mFeCO3 = 3,15.10-3. 116 = 0,3654g
%FeCO3 = (0,3654/0,6). 100% = 60,9%
→ Đáp án C
Câu 25. Chỉ dùng quỳ tím thì nhận ra được bao nhiêu dung dịch trong số bốn dung dịch mất nhãn: BaCl2, NaOH, Al(NH4)(SO4)2- và KHSO4?
A. 1 B. 2
C. 3 D. 4
Lời giải:
- Dùng quỳ tím nhận ra dung dịch NaOH (màu xanh) và dung dịch BaCl2 (màu tím).
- Còn dung dịch KHSO4 và Al(NH4)(SO4)2 đều làm quỳ tím hóa đỏ
+ KHSO4: không có hiện tượng
+ Al(NH4)(SO4)2: có khí mùi khai và kết tủa trắng tan trong kiềm dư.
→ Đáp án D
Câu 26. Để xác định hàm lượng FeCO3 trong quặng xi đe rit, người ta làm như sau: còn 0,6g mẫu quặng, chế hóa nó theo một quy trình hợp lí, thu được FeSO4 trong môi trường H2SO4 loãng. Chuẩn đọ dung dịch thu được bằng dung dịch chuẩn KMnO4 0,025M thì dùng vừa hết 25,2ml. % theo khối lượng của FeCO3 là:
A. 12,18% B. 24,26%
C. 60,9% D. 30,45%
Lời giải:
nKMnO4 = (0,025.25,2)/1000 = 6,3.10-4 mol
Phương trình phản ứng:
10FeSO4 (3,15.10-3) + 8H2SO4 + 2KMnO4 (6,3.10-4) → 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
mFeCO3 = 3,15.10-3. 116 = 0,3654g
%FeCO3 = (0,3654/0,6). 100% = 60,9%
→ Đáp án C
Câu 27. Trong nước tự nhiên thường có lẫn những lượng nhỏ các muối Ca(NO3)2, Mg(NO3)2, Ca(HCO3)2 và Mg(HCO3)2. Có thể dùng một hóa chất nào sau đây để loại được tất cả các muối trên?
A. NaOH B. Na2CO3
C. NaHCO3 D. K2SO4
Lời giải:
Khi cho Na2CO3 vào loại nước trên thì sẽ tạo kết tủa trắng CaCO3 và MgCO3
→ Đáp án B
Câu 28. Có 3 khí SO2, CO2, H2S. Chỉ dùng một hóa chất nào sau đây để phân biệt được cả 3 khí trên?
A. Dung dịch Ca(OH)2.
B. Dung dịch Ba(OH)2.
C. Dung dịch Br2
D. Dung dịch HCl.
Lời giải:
SO2 (nâu) + Br2 + 2H2O → 2HBr (không màu) + H2SO4
H2S + Br2 → 2HBr + S↑ (vàng)
→ Đáp án C
Câu 29. Cho các kim loại: Ba, Mg, Fe, Al và Ag. Nếu chỉ dùng H2SO4 loãng, có thể nhận biết được những kim loại nào ở trên?
A. Ba, Mg
B. Fe, Al
C. Al, Ag
D. Cả 5 kim loại
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch H2SO4 loãng lần lượt vào các mẩu thử.
- Kim loại không tan là Ag, các kim loại còn lại tan và tạo khí H2 và các dung dịch muối.
- Trường hợp tạo kết tủa là Ba. Lọc bỏ kết tủa rồi lấy dung dịch nước lọc có chứa Ba(OH)2 cho tác dụng với các dung dịch muối ở trên.
+ Dung dịch tạo kết tủa trắng xanh rồi hóa nâu là FeSO4.
⇒ kim loại ban đầu là Fe.
FeSO4 + Ba(OH)2 → BaSO4 + Fe(OH)2
4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
+ Dung dịch tạo kết tủa keo trắng rồi tan dần là Al2(SO4)3 ⇒ kim loại ban đầu là Al.
Al2(SO4)3 + 3Ba(OH)2 → 3BaSO4 + 2Al(OH)3
2Al(OH)3 + Ba(OH)2 → Ba[Al(OH)4]2
+ Dung dịch tạo kết tủa trắng là MgSO4 ⇒ kim loại ban đầu là Mg.
MgSO4 + Ba(OH)2 → BaSO4 + Mg(OH)2
→ Đáp án D
Câu 30. Có 5 bình mất nhãn, chứa riêng biệt các khí SO2, SO3, N2, CH3NH2 và NH3. Nếu chỉ dùng quỳ tím ẩm thì có thể nhận ra bình chứa khí:
A. SO2 B. SO3
C. N2 D. NH3
Lời giải:
SO2 và SO3 làm quỳ tím ẩm hóa đỏ.
CH3NH2 và NH3 làm quỳ tím hóa xanh.
N2 không làm đổi màu quỳ tím.
→ Đáp án C
Câu 31. Lấy 25ml dung dịch A gồm FeSO4 và Fe2(SO4)3 rồi chuẩn độ bằng dung dịch hỗn hợp KMnO4 0,025M thì hết 18,10ml. Mặt khác, thêm lượng dư dung dịch NH3 vào 25ml dung dịch A thì thu được kết tủa, lọc kết tủa rồi nung đỏ trong không khí ở nhiệt độ cao đến khối lượng không đổi, cân được 1,2g. Nồng độ mol/l của FeSO4 và Fe2(SO4)3 lần lượt là:
A. 0,091 và 0,25 B. 0,091 và 0,265
C. 0,091 và 0,255 D. 0,087 và 0,255
Lời giải:
Ta có:
nFeSO4 = 5.nKMnO4 = 2,2615.10-3 mol
CM FeSO4 = 2,2625/0,025 = 0,091M
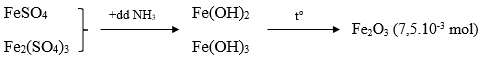
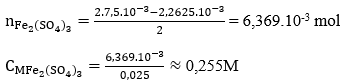
→ Đáp án C
Câu 32. Chuẩn độ 20 ml dung dịch HCl chưa biết nồng độ đã dùng hết 17 ml dung dịch NaOH 0,12M. Xác định nồng độ mol của dung dịch HCl.
A. 0,102M B. 0,12M
C. 0.08M D. 0,112M
Lời giải:
PTHH: HCl + NaOH → NaCl + H2O
nNaOH = 0,017. 0,12 = 0,00204(mol)
Theo PT: nHCl = nNaOH = 0,00204 mol
Nồng độ mol của dung dịch HCl là: 0,00204/0,02 = 0,102(M)
→ Đáp án A
Câu 33. Để tách riêng ion Zn2+, Cu2+, Fe2+ ra khỏi hỗn hợp thì có thể dùng các hóa chất nào sau đây?
A. Các dung dịch KOH, NH3, H2SO4.
B. Các dung dịch NH3, H2SO4, HCl.
C. Các dung dịch H2SO4, KOH, BaCl2.
D. Các dung dịch H2SO4, NH3, HNO3.
Lời giải:
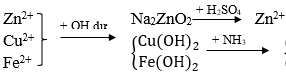
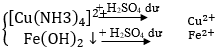
→ Đáp án A
Câu 34. Có dung dịch hỗn hợp chứa các ion Fe3+, Al3+, Cu2+. Dùng những dung dịch nào sau đây có thể tách riêng từng ion ra khỏi hỗn hợp?
A. Dung dịch NaOH, NH3.
B. Dung dịch NaOH, NH3, HCl
C. Dung dịch NaOH, HCl, H2SO4
D. Dung dịch Ba(OH)2, NaOH, NH3.
Lời giải:
Tách các chất theo sơ đồ sau:
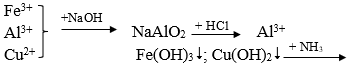
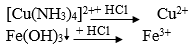
→ Đáp án B
Câu 35. Có 5 dung dịch mất nhãn gồm CuCl2, NaNO3, Mg(NO3)2; NH4NO3 và Fe(NO3)3. Có thể dùng kim loại nào sau đây để phân biệt cả 5 dung dịch?
A. Na B. Fe
C. Cu D. Ag
Lời giải:
Dùng Na: Na + H2O → NaOH + 1/2 H2
Sau đó: CuCl2 + 2NaOH → Cu(OH)2↓ (xanh) + 2NaCl
Mg(NO3)2 + 2NaOH → Mg(OH)2↓ (trắng) + 2NaNO3
NH4NO3 + NaOH → NaNO3 + NH3↑ + H2O
Fe(NO3)3 + 3NaOH → Fe(OH)3↓ (nâu đỏ) + 3NaNO3
→ Đáp án A
Câu 36. Có 6 lọ hóa chất bị mất nhãn đựng riêng biệt sáu dung dịch Na2CO3, NH4Cl, MgCl2, AlCl3, FeSO4 và Fe2(SO4)3. Bằng phương pháp hóa học và chỉ dùng một thuốc thử nào sau đây có thể nhận biết được cả sáu lọ hóa chất trên?
A. Dung dịch HCl B. Dung dịch NH3
C. Dung dịch NaOH D. Dung dịch H2SO4
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch NaOH lần lượt vào các mẩu thử.
- NH4Cl: tạo khí mùi khai NH3
- MgCl2: tạo kết tủa trắng Mg(OH)2
- AlCl3: tạo kết tủa keo trắng Al(OH)3 tan trong kiềm dư
- FeSO4: tạo kết tủa trắng xanh Fe(OH)2 bị hóa nâu trong không khí
- Fe2(SO4)3: tạo kết tủa nâu đỏ Fe(OH)3
→ Đáp án C
Câu 37. Khí CO2 có lẫn tạp chất là khí HCl. Để loại tạp chất HCl đó nên cho khí CO2 đi qua dung dịch nào sau đây là tốt nhất?
A. Dung dịch NaOH dư.
B. Dung dịch Na2CO3 dư.
C. Dung dịch NaHCO3 dư.
D. Dung dịch AgNO3 dư.
Lời giải:
Vì NaHCO3 vừa loại được HCl lại tạo ra được một lượng CO2 mới.
NaHCO3 + HCl → NaCl + CO2↑ + H2O
→ Đáp án C
Câu 38. Cho năm lọ mất nhãn đựng các dung dịch: KNO3, Cu(NO3)2, FeCl3 và NH4Cl. Có thể dùng hóa chất nào sau đây để nhận biết chúng?
A. Dung dịch NaOH dư
B. Dung dịch AgNO3
C. Dung dịch Na2SO4
D. Dung dịch HCl
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm.
Cho dung dịch NaOH lần lượt vào các mẩu thử.
- Mẩu thử tạo kết tủa xanh là Cu(NO3)2.
Cu(NO3)2 + 2NaOH → Cu(OH)2 + 2NaNO3
- Mẩu thử tạo kết tủa nâu đỏ là FeCl3.
FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl
- Mẩu thử tạo kết tủa keo trắng tan trong kiềm dư là AlC13.
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl
Al(OH)3 + NaOH → Na[Al(OH)4]
- Mẩu thử có khí mùi bay ra là NH4Cl.
NH4Cl + NaOH → NaCl + NH3 + H2O
→ Đáp án A
Câu 39. Cho ba hợp kim: Cu-Ag, Cu-Al, Cu-Zn. Thuốc thử nào sau đây có thể được dùng để phân biệt ba hợp kim trên?
A. HCl và NaOH
B. HNO3 và NH3
C. H2SO4 và NaOH
D. H2SO4 loãng và NH3
Lời giải:
Trích mẩu thử cho mỗi lần thí nghiệm. Cho dung dịch H2SO4 lần lượt vào các mẩu thử.
- Hợp kim nào không có khí là Cu-Ag.
- Cho dung dịch NH3 vào dung dịch thu được trong hai trường hợp còn lại.
+ Trường hợp tạo kết tủa keo trắng và không tan trong NH3 dư ⇒ hợp kim là Cu-Al.
3Al + 3H2SO4 → Al2(SO4)3 + 3H2
Al2(SO4)3 + 6NH3 + 6H2O → 2Al(OH)3 + 3(NH4)2SO4
+ Trường hợp tạo kết tủa rồi tan trong NH3 dư ⇒ hợp kim ban đầu là Cu-Zn.
Zn + H2SO4 → ZnSO4 + H2
ZnSO4 + 2NH3 + 2H2O → Zn(OH)2 + (NH4)2SO4
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2
→ Đáp án D
Câu 40. Để phân biệt hai khí SO2 và H2S thì nên sử dụng thuốc thử nào dưới đây?
A. Dung dịch KMnO4
B. Dung dịch Br2
C. Dung dịch CuCl2
D. Dung dịch NaOH
Lời giải:
H2S tạo kết tủa đen với CuCl2.
H2S + CuCl2 → CuS + 2HCl
→ Đáp án C

