Cách giải bài tập về Chuỗi phản ứng hóa học của kim loại hay, chi tiết - Hoá học lớp 12
Cách giải bài tập về Chuỗi phản ứng hóa học của kim loại hay, chi tiết
Với Cách giải bài tập về Chuỗi phản ứng hóa học của kim loại hay, chi tiết Hoá học lớp 12 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập Chuỗi phản ứng hóa học của kim loại từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

A. Phương pháp & Ví dụ
Lý thuyết và Phương pháp giải
Nắm chắc các tính chất hóa học chung và các tính chất đặc trưng của từng nhóm kim loại để vận dụng viết phương trình phản ứng.
Ví dụ minh họa
Bài 1: Hoàn thành sơ đồ phản ứng sau:
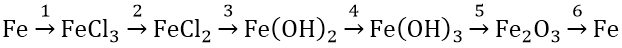
Hướng dẫn:
(1) 2Fe + Cl2 → 2FeCl3
(2) 2FeCl3 + Fe → 3FeCl2
(3) FeCl2 + 2NaOH → Fe(OH)2 + NaCl
(4) 4Fe(OH)2 + O2 + 2H2O → 4Fe(OH)3
(5) 2Fe(OH)3 −tº→ Fe2O3 + 3H2O
(6) Fe2O3 + 2Al −tº→ 2Fe + Al2O3
Bài 2: Hoàn thành phương trình phản ứng theo sơ đồ sau:
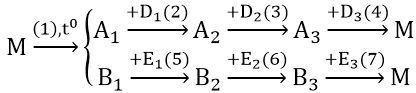
Cho biết: A1 là oxit kim loại A có điện tích hạt nhân là: 3,2.10-18 Culong; B1 là oxit phi kim B có cấu hình electron ở lớp vỏ ngoài cùng là 2s22p2
Hướng dẫn:
Số điện tích hạt nhân của A = (3,2.10-18)/(1,6.10-19) = 20(Ca)
Vậy A1 là CaO.
B ở chu kì 2, nhóm IV A ⇒ (B là cacbon). Vậy B1 là CO2
Các phản ứng:
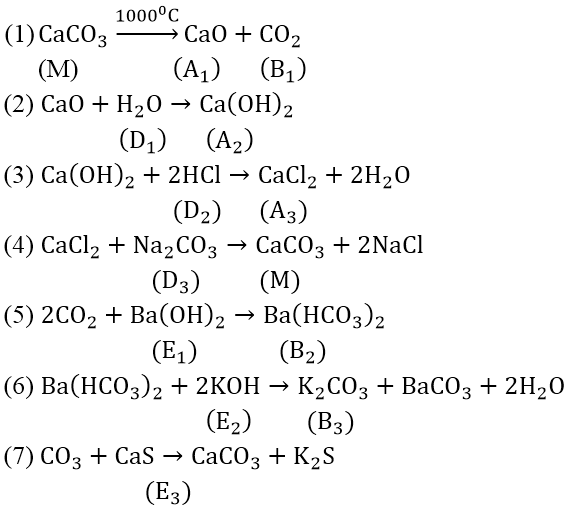
Bài 3: Hoàn thành sơ đồ phản ứng sau:
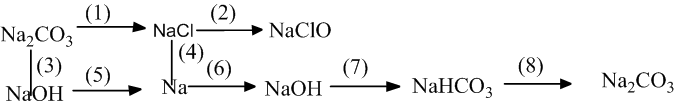
Hướng dẫn:

B. Bài tập trắc nghiệm
Bài 1: Cho các chất sau: Fe, FeCl2, FeCl3, FeSO4, Fe2(SO4)3, FeO, Fe2O3. Những chất có cả tính oxi hóa và tính khử là:
A. Fe, FeO, Fe2O3. B. FeO, FeCl2, FeSO4.
C. Fe, FeCl2, FeCl3. D. Fe, FeSO4, Fe2(SO4)3.
Lời giải:
Đáp án: B
Bài 2: Cho sơ đồ sau:
Fe → FeCl2 → Fe(OH)2 → Fe(OH)3 → Fe2O3 → Fe → FeCl3.
Số phương trình phản ứng oxi hóa - khử trong dãy là:
A. 3 B. 4 C. 5 D. 6
Lời giải:
Đáp án: B
Những phản ứng có sự thay đổi số oxi hóa là phản ứng oxi hóa – khử
Fe + 2HCl → FeCl2 + H2
FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl
4Fe(OH)2 + O2 + 2H2O → 4 Fe(OH)3
2Fe(OH)3 −tº→ Fe2O3 + 3H2O
Fe2O3 + 2Al −tº→ 2Fe + Al2O3
Fe + Cl2 → FeCl3
Bài 3: Phương trình phản ứng nào sau đây viết sai?
A. FeCO3 + 2HNO3 → Fe(NO3)2 + CO2 + H2O
B. 2FeCl2 + Cl2 → 2FeCl3
C. 2FeCl3 + 2KI → 2FeCl2 + 2KCl + I2
D. Fe2O3 + 6HNO3 đặc −tº→ 2Fe(NO3)3 + 3H2O.
Lời giải:
Đáp án: A
3FeCO3 + 10HNO3 → 3Fe(NO3)3 + 5H2O + NO + 3CO2
Bài 4: Để khử ion Fe3+ trong dung dịch thành ion Fe2+ có thể dùng dư chất nào sau đây?
A. Mg B. Cu C. Ba D. Na
Lời giải:
Đáp án: B
Cu + 2Fe3+ → Cu2+ + 2Fe2+
Bài 5: Cho từng chất: Fe, FeO, Fe(OH)2, Fe(OH)3, Fe3O4, Fe2O3, Fe(NO3)2, Fe(NO3)3, FeSO4, Fe2(SO4)3, FeCO3 lần lượt phản ứng với HNO3 đặc nóng. Số phản ứng oxi hóa - khử là:
A. 5 B. 6 C. 7 D. 8
Lời giải:
Đáp án: C
Bài 6: Khi nung nóng hỗn hợp các chất Fe(NO3)2, Fe(OH)2 và FeCO3 trong không khí đến khối lượng không đổi thu được một chất rắn là:
A. FeO B. Fe C. Fe3O4 D. Fe2O3
Lời giải:
Đáp án: D
Bài 7: Cho sơ đồ sau: FeS2 → X → Y → Z → Fe
Các chất X, Y, Z lần lượt là:
A. FeS, Fe2O3, FeO. B. Fe3O4, Fe2O3, FeO.
C. Fe2O3, Fe3O4, FeO. D. FeO, Fe3O4, Fe2O3.
Lời giải:
Đáp án:C
2FeS2 + 11/2O2 −tº→ Fe2O3 + 4SO2
3Fe2O3 + CO −tº→ 2Fe3O4 + CO2
Fe3O4 + CO −tº→ 3FeO + CO2
FeO + CO −tº→ Fe + CO2

