Dạng bài tập phản ứng este hóa của Amino Axit - Hoá học lớp 12
Dạng bài tập phản ứng este hóa của Amino Axit
Với Dạng bài tập phản ứng este hóa của Amino Axit Hoá học lớp 12 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập phản ứng este hóa của Amino Axit từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

PHẢN ỨNG ESTE HÓA CỦA AMINO AXIT
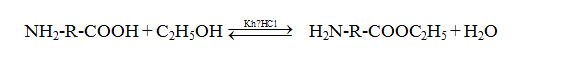
Ví dụ
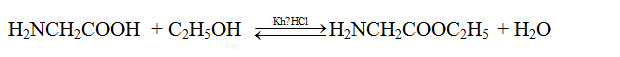
Sản phẩm của phản ứng este hóa: Este của aminoaxit có dạng NH2-R-COOR' vừa có thể phản ứng trong môi trường axit vừa phản ứng trong môi trường bazơ nhưng đây không phải là chất lưỡng tính:
NH2-R-COOR' + HCl → NH3Cl-R-COOR'
NH2-R-COOR' + NaOH → NH2-R-COONa + R'OH
Bài tập minh họa
Câu 1:Aminoaxit có khả năng tham gia phản ứng este hóa vì:
A. Amino axit là chất lưỡng tính
B. Aminoaxit chứa nhóm chức –COOH
C. Aminoaxit chứa nhóm chức –NH2
D. Tất cả đều sai
Lời giải:
Amino axit chứa nhóm –COOH trong phân tử
⇒ Mang đầy đủ tính chất của axit cacbonxylic, do đó amino axit có phản ứng este hóa.
→ Đáp án B
Câu 2:Este A được điều chế từ amino axit B (chỉ chứa C, H, O, N) và ancol metylic. Tỉ khối hơi của A so với H2 là 44,5. Đốt cháy hoàn toàn 8,9g este A thu được 13,2g CO2; 6,3g H2O và 1,12 lít N2 (đktc). Công thức cấu tạo thu gọn của A, B lần lượt là:
A. CH2(NH2)COOCH3; CH2(NH2)COOH.
B. CH(NH2)2COOH; CH(NH2)2COOCH3.
C. CH2(NH2)COOH; CH2(NH2)COOCH3.
D. CH(NH2)2COOCH3; CH(NH2)2COOH.
Lời giải:
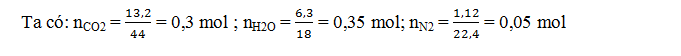
⇒ Trong A: nC = 0,3 mol; nH = 0,7 mol; nN = 0,1 mol
8,9 g este A có mO = 8,9 – 12.0,3 – 1. 0,7 – 14. 0,1= 3,2 g
⇒ nO = 0,2 mol
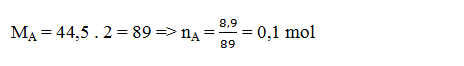
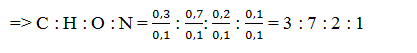
CTPT của A là: C3H7NO2
A tạo từ amino axit B và ancol CH3OH ⇒ CTCT của este A là: H2NCH2COOCH3
⇒ amino axit B là H2NCH2COOH ( glyxin)
→ Đáp án
Câu 3:Hợp chất hữu cơ X (C5H11O2N) tác dụng với dung dịch NaOH dư, đun nóng thu được muối natri của α-amino axit và ancol. Số công thức cấu tạo của X là:
A. 6
B. 2
C. 5
D. 3
Lời giải:
Cấu tạo của X có thể là:
CH3-CH2-CH(NH2)-COO-CH3
(CH3)2C(NH2)-COO-CH3
CH3-CH(NH2)-COO-C2H5
NH2-CH2-COO-CH2-CH2-CH3
NH2-CH2-COO-CH(CH3)2
→ Đáp án C

