Phương pháp tăng giảm khối lượng trong hóa học hữu cơ hay, có lời giải - Hoá học lớp 12
Phương pháp tăng giảm khối lượng trong hóa học hữu cơ hay, có lời giải
Với Phương pháp tăng giảm khối lượng trong hóa học hữu cơ hay, có lời giải Hoá học lớp 12 gồm đầy đủ phương pháp giải, ví dụ minh họa và bài tập trắc nghiệm có lời giải chi tiết sẽ giúp học sinh ôn tập, biết cách làm dạng bài tập tăng giảm khối lượng trong hóa học hữu cơ từ đó đạt điểm cao trong bài thi môn Hoá học lớp 12.

Phương pháp giải
Các dạng bài thường gặp:
+ Kim loại tác dụng với hợp chất có nhóm –OH linh động ( ancol, phenol, axit cacboxylic) → muối + H2
2R(OH)n + nNa → 2R(ONa)n + nH2
Khi chuyển 1 Na vào muối sẽ giải phóng 0,5 mol H2 tương ứng với sự tăng khối lượng là: ∆mtăng = 22n
+ Bài toán phản ứng este hóa
RCOOH + HO-R’ → RCOOR’ + H2O
m este < m muối ⇒∆m tăng = m muối – m este
m este > m muối ⇒∆m giảm = m este – m muối
+ Bài toán trung hòa: -OHaxit, phenol + kiềm
-OH + NaOH → -ONa + H2O
Cứ 1 mol axit (phenol) → muối: ∆mtăng = 22g
Ví dụ minh họa
Ví dụ 1: Khi oxi hóa hoàn toàn 2,2g một anđehit đơn chức thu được 3g axit tương ứng. Công thức anđehit là:
A. HCHO
B. C2H3CHO
C. C2H5CHO
D. CH3CHO
GiảiVí dụ:
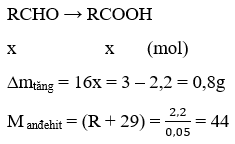
⇒R = 15 ⇒Anđehit là: CH3CHO ⇒ Đáp án D
Ví dụ 2: Oxi hóa m gam X gồm CH3CHO, C2H3CHO, C2H5CHO bằng oxi xúc tác, sản phẩm thu được sau phản ứng gồm 3 axit có khối lượng m + 3,2 gam. Cho m gam X tác dụng với lượng dư dung dịch AgNO3/NH3 thì thu được x gam kết tủa. Gía trị x là:
A. 10,8g
B. 21,6g
C. 32,4g
D. 43,2g
GiảiVí dụ:
2R−CHO + O2 → 2 R−COOH
⇒Khối lượng tăng 3,2g là khối lượng của oxi đã tham gia phản ứng
⇒n X = 2n O2 = 2. 3,2/32 = 0,2 mol
Vì các anđehit là đơn chức ( không có HCHO) ⇒n Ag = 2n X = 2.0,2 = 0,4 mol
⇒m Ag = x = 0,4.108 = 43,2g
⇒Đáp án D
Ví dụ 3: Cho 3,74g hỗn hợp 4 axit, đơn chức tác dụng với dung dịch Na2CO3 thu được V lít khí CO2 (đktc) và dung dịch muối. Cô cạn dung dịch thì thu được 5,06g muối. Gía trị V là:
A. 0,224 lít
B. 0,448 lít
C. 1,344 lít
D. 0,672 lít
Giải
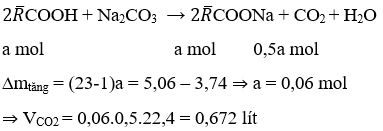
⇒Đáp án D
Ví dụ 4: Cho 2,02g hỗn hợp hai ancol đơn chức, đồng đẳng kế tiếp tác dụng với Na vừa đủ thu được 3,12g muối khan. Công thức phân tử của hai ancol là:
A. CH3OH, C2H5OH
B. C2H5OH, C3H7OH
C. C3H7OH, C4H9OH
D. C4H9OH, C5H11OH
Giải
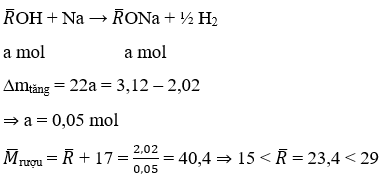
⇒2 rượu là: CH3OH và C2H5OH
⇒Đáp án A
Ví dụ 5: Đốt cháy hoàn toàn m gam hỗn hợp các este no, đơn chức, mạch hở. Dẫn toàn bộ sản phẩm cháy vào bình đựng dung dịch Ba(OH)2 dư thấy khối lượng bình tăng 1,55g. Khối lượng kết tủa thu được là:
A. 2,5g
B. 4,925g
C. 6,94g
D. 3,52g
GiảiVí dụ:
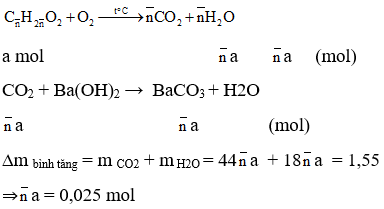
⇒m↓= 0,025.197 = 4,925g ⇒Đáp án B
Bài tập tự luyện
Bài 1: Cho 5,9 gam amin đơn chức X tác dụng vừa đủ với dung dịch HCl sau khi phản ứng xảy ra hoàn toàn thu được dung dịch Y. Làm bay hơi dung dịch Y được 9,55g muối khan. Số công thức cấu tạo ứng với công thức phân tử X là:
A. 5
B. 4
C. 2
D. 3
Lời giải:
Hướng dẫn giải
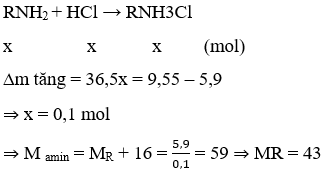
⇒X: C3H7NH2
CH3 – CH2 – CH2 – NH2; (CH3)2CHNH2; CH3NHCH3CH2; (CH3)3N
⇒Đáp án B
Bài 2: Trong phân tử amino axit X có 1 nhóm amino và 1 nhóm cacboxyl. Cho 15,0g X tác dụng vừa đủ với dung dịch NaOH. Cô cạn dung dịch sau phản ứng thu được 19,4g muối khan. Công thức X là:
A. H2NC3H6COOH
B. H2NCH2COOH
C. H2NC2H4COOH
D. H2NC4H8COOH
Lời giải:
Hướng dẫn giải:
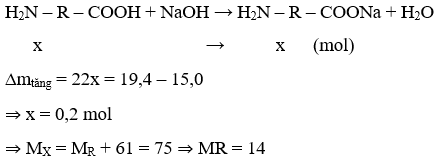
⇒X là: H2NCH2COOH
⇒Đáp án B
Bài 3: Đốt cháy hoàn toàn 4,40g chất hữu cơ X đơn chức thu được sản phảm cháy gồm 4,48 lít CO2 (đktc) và 3,60g H2O. Nếu cho 4,40g X tác dụng với dung dịch NaOH vừa đủ đến khi phản ứng hoàn toàn thu được 4,80g muối axit hữu cơ Y và chất hữu cơ Z. Tên của X là:
A. Etyl propionat
B. Metyl propionat
C. Isopropyl axetat
D. Etyl axetat
Lời giải:
Hướng dẫn giải:
n CO2 = n H2O = 0,2 mol ⇒X là este no đơn chức
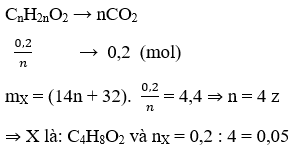
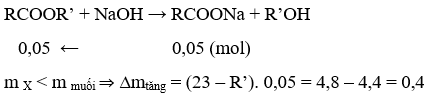
⇒R’ = 15 ⇒Công thức cấu tạo của X là: C2H5COOCH3
⇒Đáp án B
Bài 4: Hỗn hợp X gồm HCOOH và CH3COOH ( tỉ lệ 1: 1). Lấy 5,30 gam hỗn hợp X tác dụng với 5,75g C2H5OH (xúc tác H2SO4 đặc) thu được m gam este ( hiệu suất của các phản ứng este hòa đều bằng 80%). Gía trị của m là:
A. 10,12g
B. 6,48g
C. 16,20g
D. 8,10g
Lời giải:
Hướng dẫn giải:

⇒Đáp án B
Bài 5: Hỗn hợp X có khối lượng 25,1g gồm 3 chất axit axetic, axit acrylic và phenol. Lượng hỗn hợp X trên được trung hòa vừa đủ bằng 100ml dung dịch NaOH 3,5M. Khối lượng ba muối thu được sau phản ứng trung hòa là:
A. 32,80g
B. 33,15g
C. 34,47g
D. 31,52g
Lời giải:
Hướng dẫn giải:
n NaOH = 0,35 mol
X: -OH + NaOH → ONa
Ta thấy cứ 1 mol X ( chứa 1 nhóm –OH) khi tác dụng với 1mol NaOH thu được 1 mol muối tăng 22g so với khối lượng axit
⇒Với 0,35mol NaOH khối lượng muối tăng = 0,35.22 = 7,7g
⇒ m muối = m X + 7,7 = 25,1 + 7,7 = 32,8g
⇒Đáp án A
Bài 6: X là một α- aminoaxit chỉ chứa 1 nhóm –NH2 và 1 nhóm –COOH. Cho 0,445g X phản ứng vừa đủ với NaOH tạo ra 0,555g muối. Tên gọi của X là:
A. Glyxin
B. Alanin
C. Valin
D. Gluxin
Lời giải:
Hướng dẫn giải:
X: -COOH + NaOH → -COONa + H2O
Ta có: 1mol X + 1 mol NaOH → 1 mol muối và khối lượng muối tăng so với khối lượng X là: 23-1=22g
Theo đề bài: ∆mtăng = 0,555 – 0,445 = 0,11g
⇒nX = 0,11: 22 = 0,005 mol
MX = 0,445: 0,005 = 89 ⇒X là glyxin ( NH2 – CH2 – COOH)
⇒Đáp án A
Bài 7: Thủy phân hoàn toàn 1,76g X đơn chức bằng 1 lượng vừa đủ dung dịch NaOH đun nóng được 1,64g muối Y và m gam ancol Z. Lấy m gam Z tác dụng với lượng dư CuO nung nóng đến phản ứng hoàn toàn thấy lượng chất rắn giảm 0,32g. Tên gọi của X là:
A. Etyl fomat
B. Etyl propionat
C. Etyl axetat
D. Metyl axetat
Lời giải:
Hướng dẫn giải:
X là este: RCOOR’
∆m giảm = m axit – m muối = 1,76 – 1,64 = 0,12 mol
RCOOR’ + NaOH → RCOONa + R’OH
Ta có: Cứ 1mol X + 1 mol NaOH tạo ra 1 mol muối. Khối lượng muối giảm so với khối lượng axit là: R’ - 23
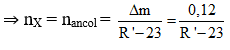
R’OH + CuO → Cu
Ta thấy: 1 mol ancol + 1 mol CuO tạo ra 1 mol Cu. Và khối lượng chất rắn giảm chính là khối lượng O = 16g
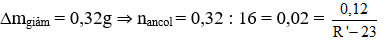
⇒R’ = 29: - C2H5
nX = 0,02 ⇒MX = 1,76: 0,02 = 88
⇒R = 15: -CH3
Vậy X là: CH3COOC2H5: etylaxetat ⇒Đáp án C
Bài 8: Để trung hòa 7,4g hỗn hợp 2 axit hữu cơ đơn chức cần 200ml dung dịch NaOH 0,5M. Khối lượng muối thu được khi cô cạn dung dịch là:
A. 9,6g
B. 6,9g
C. 11,4g
D. 5,2g
Lời giải:
Hướng dẫn giải:
n NaOH = 0,5.0,2 = 0,1 mol
Axit đơn chức: RCOOH
RCOOH + NaOH → RCOONa
Ta thấy cứ 1 mol axit + 1 mol NaOH → tạo ra 1 mol muối, khối lượng muối tăng so với axit là: 23 – 1 = 22g
⇒0,1 mol NaOH: ∆m tăng = 0,1.22 = 2,2g
m muối = m axit + ∆m tăng = 7,4 + 2,2 = 9,6g ⇒Đáp án A
Bài 9: Cho một anken X tác dụng hết với H2O ( H+, t°C) được chất hữu cơ Y, đồng thời khối lương bình đựng nước ban đầu tăng 4,2g. Cũng cho một lượng X như trên tác dụng với HBr vừa đủ, thu được chất Z, thấy khối lượng Y,Z thu được khác nhau 9,45g ( giả sử các phản ứng xảy ra hoàn toàn). Công thức phân tử của X là:
A. C2H4
B. C3H6
C. C4H8
D. C5H10
Lời giải:
Hướng dẫn giải:
Gọi anken là CnH2n
Ta có mbình nước tăng = manken = 4,2g
Y: CnH2n+1OH và Z: CnH2n+1Br
Ta có: Cứ 1 mol X → 1 mol Y và 1 mol Z và khối lượng Z lớn hơn khối lượng Y là 80 – 17 = 63g
Theo đề bài mZ – mY = 9,45g
⇒nX = 9,45: 63 = 0,15 mol
MX = 4,2: 0,15 = 28 ⇒X là: C2H4
⇒Đáp án A
Bài 10: Dẫn 130cm3 hỗn hợp X gồm 2 hiđrocacbon mạch hở qua dung dịch Br2 dư khí thoát ta khỏi bình có thể tích 100cm3, biết d X/He = 5,5 và phản ứng xảy ra hoàn toàn. Hai hiđrocacbon cần tìm là:
A. Metan, propen
B. Metan, axetilen
C. Etan, propen
D. Metan, xiclopropan
Lời giải:
Hướng dẫn giải:
100cm3 thoát ra khỏi bình brom ⇒Hỗn hợp X có ankan; Vankan = 100cm3
d X/He = 5,5 ⇒MX = 22 ⇒Trong X hợp chất có phân tử khối < 15
⇒X có CH4 (16) và V CH4 = 100cm3
Gọi hiđrocacbon lại là CxHy; VCxHy = 130 – 100 = 30cm3
Ta có sơ đồ đường chéo:
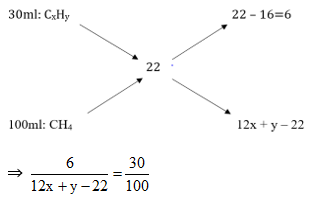
⇒12x + y = 42
⇒x = 3; y = 6
Vậy X gồm: C3H6 và CH4
⇒Đáp án A

