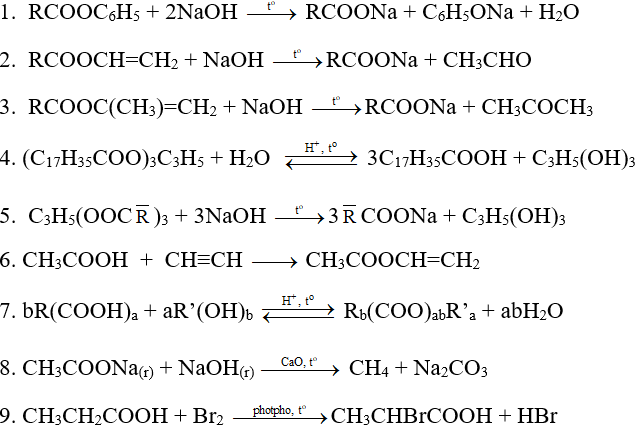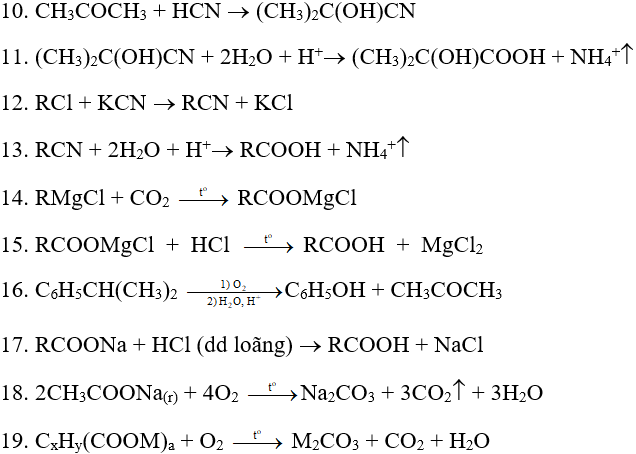Tính chất của Chất giặt rửa hay, chi tiết nhất - Hoá học lớp 12
Tính chất của Chất giặt rửa hay, chi tiết nhất
Tài liệu Tính chất của Chất giặt rửa hay, chi tiết nhất Hoá học lớp 12 sẽ tóm tắt kiến thức trọng tâm về Tính chất của Chất giặt rửa từ đó giúp học sinh ôn tập để nắm vứng kiến thức môn Hoá học lớp 12.

I. Khái niệm và tính chất của chất giặt rửa
1. Khái niệm
- Chất giặt rửa: là những chất khi dùng cùng với nước có tác dụng làm sạch các chất bẩn bám trên vật rắn mà không gây ra phản ứng hóa học với các chất đó.
- Một số khái niệm liên quan:
+ Chất tẩy màu: làm sạch các vết màu bẩn nhờ những phản ứng hóa học. VD: nước javel.
+ Chất ưa nước: là những chất tan tốt trong nước như: metanol, etanol, axit axetic, muối axetat kim loại kiềm…
+ Chất kị nước: là những chất hầu như không tan trong nước, như hidrocacbon, dẫn xuất halogen…
+ Chất kị nước thì ưa dầu mỡ, tức là tan tốt vào dầu mỡ. Chất ưa nước thì thường kị dầu mỡ, tức là không tan trong dầu mỡ.
2. Đặc điểm cấu trúc phân tử muối natri của axit béo
Cấu trúc hóa học chung cho phân tử chất giặt rửa: gồm 1 đầu ưa nước là nhóm COO-Na+ gắn với 1 đuôi dài ưa dầu mỡ (kị nước) là nhóm -CxHy.
3. Cơ chế hoạt động
Đuôi ưa dầu mỡ trong phân tử muối natri của axit béo thâm nhập vào vết dầu bẩn, còn đầu ưa nước lại có xu hướng kéo ra phía các phân tử nước. Kết quả là vết dầu bị phân chia thành những hạt rất nhỏ được giữ chặt bởi các phân tử muối natri, không bám vào vật rắn nữa mà phân tán vào nước rồi bị rửa trôi đi.
II. Xà phòng
1. Khái niệm
Xà phòng là muối của Na hoặc K với axit béo cao và chất phụ gia.
+ Xà phòng rắn là hỗn hợp muối natri của các axit béo, chủ yếu là natri stearat, natri panmiat.
+ Các xà phòng của Kali đều là xà phòng lỏng.
+ Xà phòng thơm là hỗn hợp xà phòng và tinh dầu thơm hoặc creazol.
2. Sản xuất xà phòng
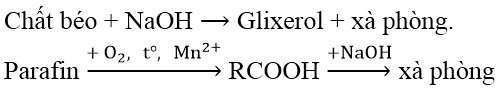
3. Thành phần xà phòng
- Thành phần chính của xà phòng là các muối natri/kali của axit béo, thường là natri stearat C17H35COONa, natripanmitat C15H31COONa, natrioleat C17H33COONa… Các phụ gia thường gặp là chất màu, chất thơm.
- Xà phòng dùng trong tắm gội, giặt giũ…
- Ưu điểm là không gây hại cho da và môi trường do dễ bị phân hủy bởi vi sinh vật có trong thiên nhiên.
- Nhược điểm là khi dùng với nước cứng thì các muối canxi stearat, canxi panmitat…sẽ kết tủa làm giảm tác dụng giặt rửa và ảnh hưởng đến chất lượng vải sợi.
III. Chất giặt rửa tổng hợp
1. Sản xuất chất giặt rửa
- Chất giặt rửa tổng hợp được điều chế từ các sản phẩm của dầu mỏ.
- VD: oxi hóa parafin được axit cacboxylic, hidro hóa axit thu được ancol, cho ancol phản ứng với H2SO4 rồi trung hòa thì được chất giặt rửa loại ankyl sunfat:
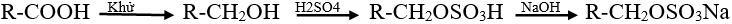
2. Thành phần chất giặt rửa
- Các chế phẩm như bột giặt, kem giặt… bao gồm các thành phần: chất giặt rửa tổng hợp, các phụ gia chất thơm, chất màu, còn có thể có chất tẩy trắng như natri hipoclorit. Chất này có hại cho da khi giặt bằng tay.
- Ưu điểm của chất giặt rửa tổng hợp là dùng được với nước cứng vì chúng ít bị kết tủa bởi ion canxi.
- Nhược điểm: Những chất giặt rửa tổng hợp có chứa gốc hidrocacbon phân nhánh gây ô nhiễm môi trường, vì chúng rất khó bị các vi sinh vật phân hủy.
3. Tác dụng giặt rửa của xà phòng và chất tẩy rửa tổng hợp
- Xà phòng và chất giặt rửa tổng hợp có tác dụng làm giảm sức căng bề mặt của nước, làm cho nước dễ thấm ướt các giọt dầu, mỡ và các chất bẩn bám trên bề mặt. Khi giặt, rửa bằng xà phòng, gốc R của phân tử xà phòng bám vào chất bẩn, nhóm phân cức (-COONa) chuyển (hoàn toàn) chất bẩn vào nước dưới dạng nhũ tương ứng hay huyền phù, do đó làm sạch vật giặt, rửa.
- Xà phòng và chất giặt rửa tổng hợp bao gồm 2 phần:
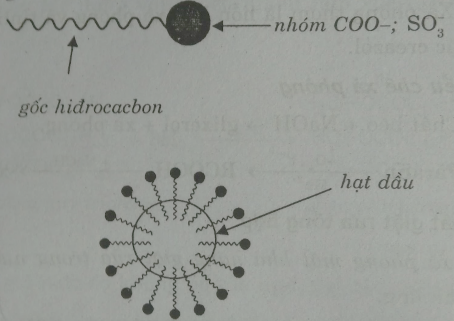
+ Phần kị nước: gốc hi đrocacbon: R- hoặc R-C6H4- nhưng dễ tan trong vết bẩn.
+ Phần ưa nước: các nhóm SO32-, COO- do tạo liên kết hiđro với nước.
- Anion SO32-, COO- định hướng thẳng vào bề mặt dung dịch, cho nên khi giặt rửa các chất bẩn, chúng phân chia thành những hạt rất nhỏ không còn khả năng bám vào vật giặt và bị cuốn trôi theo nước.
IV. Một số phản ứng hóa học thường gặp